сплав
В металлургии сплав (от латинского ligare ' связывать, объединять' ) представляет собой макроскопически однородный металлический материал, состоящий по крайней мере из двух элементов (компонентов), по крайней мере, один из которых является металлом и которые вместе имеют типичный металл. Характерные из металлической связи . С химической точки зрения существуют сплавы, которые представляют собой смеси и интерметаллические соединения с определенным стехиометрическим соотношением задействованных металлов. В целом сплавы также имеют кристаллическую структуру. Однако есть и аморфные металлические стекла .
В зависимости от типа образования сплава сплав может быть более однородным или неоднородным на микроскопическом уровне . Сплавы, которые образуют только смешанные кристаллы или исключительно интерметаллические соединения, являются гомогенными. Все остальные, состоящие из нескольких фаз, неоднородны.
Поведение элементов в сплаве и их влияние на их свойства обычно зависят от трех факторов: типа и количества легирующих компонентов, их массового соотношения в сплаве и температуры. Эти факторы определяют соответствующую поглощающую способность, то есть растворимость одного элемента в другом и образуют ли партнеры сплава смешанные кристаллы или смеси чистых кристаллов (также кристаллические смеси ) соответствующих компонентов сплава.
Глагол « сплав» происходит от латинского ligare и означает «связывать вместе», «соединяться» или «объединяться». В 17 веке , теперь немного измененный legare (с тем же значением) был принят на немецкий язык .
характеристики
Легирующий элемент может образовывать твердый раствор с базовым элементом (однофазный сплав) или несколько образуются фазами . В то время как свойства однофазных сплавов в основном определяются химическим составом, в случае многофазных сплавов на них также значительно влияет распределение фаз ( структура ). Основной металл и легирующие элементы также называют компонентами сплава. В списке легирующих элементов показаны они и их влияние на соответствующие основные металлы. Смешанные кристаллы имеют более высокую твердость и прочность на разрыв , но более низкую температуру плавления, чем основной металл. В случае металлов также падает электропроводность . Для относительно мягких чистых металлов упрочнение твердого раствора является одним из четырех возможных способов увеличения прочности с целью получения твердого материала.
Когда литой сплав затвердевает, кристаллизация не всегда завершается. Некоторые сплавы также могут улучшать свои механические свойства (прочность на разрыв, твердость, удлинение) при литье - старении в холодном или нагретом состоянии («отпуске»). В случае деформируемых сплавов рекристаллизация, которая укрепляет структуру за счет холодного старения или термообработки, является даже предпосылкой для производства полуфабрикатов.
Примеры «естественных» сплавов являются электрумом , А золото - серебро сплав, и stibarsen , сурьма - мышьяк сплава.
В «искусственных сплавах» - различие между теми, которые были намеренно сделаны в свойствах материалов (например, твердость , искомая коррозия ), чтобы изменить «основные металлы» желаемым образом, и те, которые уже непреднамеренно образуются в виде примесей ( металлургия ). При производстве могут попасть в сплав и отрицательно повлиять на свойства материала. Примерами последнего являются, среди прочего, висмут и / или мышьяк в латуни , а также висмут в сплавах AlSi , где он сильно влияет на формирование структуры.
история
Медь, олово и бронза
Медь - один из первых металлов, используемых человеком; он был обнаружен случайно от 6000 до 10000 лет назад при пожаре древесного угля, который горел особенно горячим при контакте с воздухом. Это дало название медному веку . При температуре плавления 1083 ° C он может выходить в жидкой форме из медных жил в породе. Однако при нагревании медьсодержащих оксидных руд медь можно получить только при восстановительном обжиге, то есть в присутствии древесного угля. Олово (точка плавления 232 ° C) было открыто около 5000 лет назад.
Бронза как сплав меди и олова (CuSn) является доисторической эпохой примерно с 3300 г. до н. Э. Проверено в Палестине . Бронза тверже и лучше обработана, чем медь, и дала название бронзовому веку (около 2200–800 гг. До н.э.). Посуда, инструменты , оружие и украшения изготавливались из бронзы. Колокола по сей день отливают из бронзы; столько же скульптур .
Латунь
Латунь - это сплав меди и цинка (CuZn, температура плавления 420 ° C). Цинк, в основном в форме карбоната цинка «каламин» ( смитсонит ), существует с бронзового века около 3000 г. до н.э. Используется в Вавилоне и Ассирии , в Палестине примерно с 1400 по 1000 годы до нашей эры. Долгое время латунь была важным металлом, используемым в чеканке монет . Из-за своего золотого блеска он использовался и используется для изготовления украшений и скульптур. Чем выше содержание цинка, тем светлее его цвет.
Железные сплавы
Сплавы железа использовались уже в доисторические времена , но только из метеоритов , которые часто содержат сплав железа с никелем (FeNi). Поскольку метеориты находили редко, железные предметы были соответственно ценны. В Шумеры называли его «небесный металл», то древние египтяне «черную медь с небес». Плавленое железо (признанное по отсутствию никеля) было обнаружено в Месопотамии , Анатолии и Египте и находится примерно в 3000–2000 годах до нашей эры. До нашей эры. Он был более ценным, чем золото, и использовался в основном для церемониальных целей. Железо тверже бронзы и меди, что было и важно во многих сферах применения. Улучшения в добыче и обработке железа побудили людей изготавливать из железа оружие и инструменты, такие как плуги (см. Также историю производственных технологий ). Закончился бронзовый век и начался железный век .
Классификация
В зависимости от количества компонентов в сплаве говорят о двух-, трех-, четырех- или многокомпонентном сплаве (бинарном, тройном, четвертичном или полинарном сплаве), при этом учитываются только те компоненты, которые определяют характерные свойства. Поскольку железо и сталь имеют особое значение в технологии , сплавы делятся на железные и цветные. Дальнейшие классификации вытекают из типа образования сплава, поскольку они возникают не только из-за плавления компонентов или также из-за особых свойств сплавов.
- Природные сплавы создаются под действием тепла и плавления элементов, например, внутри небесных тел . Поскольку эти сплавы не контролировались людьми, они также не подчиняются определенным им составам и свойствам.
- Сплавы железа делятся на чугун и сталь . Различие основано на содержании углерода . См. Диаграмму железо-углерод в основной статье. Особое значение имеют нержавеющие стали : легированные или нелегированные стали с особой степенью чистоты.
- Цветные сплавы (цветные сплавы; например, бронза , латунь , амальгамы , белое золото , красное золото ) - это сплавы на основе цветных металлов .
- Сплавы диффузии создаются диффузией атомов в кристаллическую решетку основных металлов. В частности, первые элементы в периодической таблице могут мигрировать в ее кристаллическую решетку из-за небольшого размера их атомов по сравнению с основным металлом . Лучшим примером диффузионного сплава является науглероживание заготовок с целью их упрочнения (см. Отжиг ).
- Сплавы Гейслера - это особые ферромагнитные сплавы, не содержащие железа, кобальта или никеля (например, Cu 2 AlMn).
- Сплавы с памятью формы - это металлы, которые возвращаются к своей первоначальной форме после деформации под действием тепла.
- Для прямой формовки используются литейные сплавы .
- Деформируемые сплавы , как «полуфабрикаты», представляют собой промежуточный продукт, предназначенный для дальнейшей прокатки, прессования или волочения.
- Заготовки, полученные спеканием ( прессование различных, тесно смешанных металлических порошков при высокой температуре) , называются псевдосплавами . Этот процесс также можно использовать для смешивания элементов, которые не растворяются друг в друге в расплавленном состоянии. Многие сплавы вольфрама z. Б. так и сделал.
Формула сплава
Чтобы идентифицировать сплав, обычно первым упоминается основной металл, за которым следуют наиболее важные компоненты в виде аббревиатуры металла с добавленным числом, которое показывает соответствующий процент ( массовые проценты ). Сплав CuZn37 (ранее известный как латунь 63 ) состоит из медной основы, к которой было добавлено 37% цинка . В случае легированной стали с железом и углеродом имеются отклонения от этой системы в зависимости от количества легирующих элементов. Во всяком случае, железо прямо никогда не упоминается. Например, сталь C37 содержит 0,37% углерода и железа.
Указание пропорций сплавов основано, среди прочего, на составе смешанных фаз согласно DIN 1310 (газовая смесь, растворы, смешанный кристалл); Основные условия регулируются.
Диаграмма состояний (диаграмма состояний, фазовая диаграмма)
Во время термического анализа серии испытаний на кристаллизацию с различными сплавами разного состава используются для регистрации точек кристаллизации или превращения кристаллов и занесения их в диаграмму «температура-состав», причем температура зависит от состава сплава.
Для бинарных систем появились три типичных вида диаграмм состояния, особенно в отношении кристаллической системы:
Двухкомпонентные системы с полной растворимостью в твердом состоянии.
При полной растворимости в твердом состоянии смешанные кристаллы образуются в любом составе. Есть две возможности для образования твердого раствора (МК), включения и замещения твердого раствора . Типичными заменителями МК являются сплавы железо-хром, железо-никель, золото-медь, золото-серебро и медь-никель. Аустенит (γ-железо-углерод) является важным образующим интеркаляции МК .
Чтобы сплав любого состава мог образовывать смешанные кристаллы с полной растворимостью в твердом состоянии, необходимы следующие требования:
- Оба металла должны иметь одинаковую кристаллическую систему (например, кубическую ).
- Константы решетки могут отличаться максимум примерно на 15%.
- Два металла должны иметь «определенное химическое сходство».
- Электроотрицательность разница должна быть «не слишком большой».
Из-за образования смешанных кристаллов, независимо от того, насколько похожи легирующие элементы , кристаллическая решетка всегда искажается, поскольку различные элементы также имеют разные атомные диаметры. Это создает напряженность; на скользящие плоскости в кристаллитах затруднены из податливых к деформациям. Таким образом, искажение решетки увеличивает твердость.
Популярным примером сплава с полной растворимостью в твердом состоянии является двухкомпонентная система Cu-Ni.

|
|
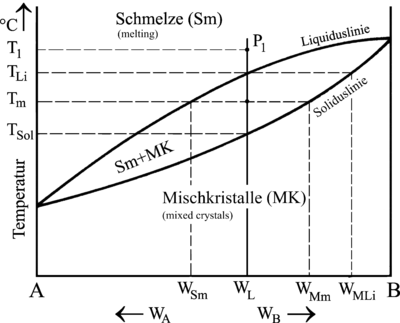
| Кривые охлаждения и диаграмма состояния сплава различного состава с образованием твердого раствора | |
В отличие от основных металлов (кривые 1.6) сплавы (кривые 2-5) затвердевают не при фиксированной температуре, а в зоне выдержки. Таким образом, температура не остается постоянной, а постепенно снижается. Однако интервалы выдержки для различных составов сплава всегда находятся между соответствующими температурами затвердевания их чистых компонентов.
Причина этого - «препятствие» кристаллизации сплава компонентом А (кривая 1), который, если бы мог, затвердевал бы при еще более низкой температуре. Компонент B, с другой стороны, «подталкивает» к затвердеванию, которое на самом деле должно было начаться раньше. Этот факт также является причиной того, что кристаллы, образующиеся во время затвердевания, изменяют свое соотношение смешивания, и только когда охлаждение является достаточно медленным ( тепловое равновесие ) до конца затвердевания, желаемое соотношение смешивания достигается за счет диффузии.
Эти составы можно прочитать на диаграмме состояний, проведя горизонтальную линию через любую точку выбранного сплава (рис. W L ) до линии солидуса . При температуре ликвидуса Т Li (начало твердения) поэтому первые кристаллы имеют состав W МСИ . Соответствующий состав остаточного расплава также можно определить таким образом, например, проведя горизонтальную линию при T m до линии ликвидуса. Таким образом, в этот момент расплав будет иметь состав W Sm, а смешанные кристаллы - состав W Mm .
С помощью диаграммы состояний и закона рычагов можно также рассчитать, насколько высока доля расплава или доля смешанных кристаллов при каждой промежуточной температуре:
|
|
M S = доля расплава |
Двухкомпонентные системы с полной нерастворимостью в твердом состоянии.
Сплавы этого типа действительно растворяются друг в друге в расплаве, но полностью разделяются во время кристаллизации. В результате получается кристаллическая смесь чистых компонентов (см. Эвтектику на микрофотографии ).

|

|
| Кривые охлаждения и диаграмма состояния сплава разного состава с раздельным кристаллообразованием | |
Даже при отдельном формировании кристаллов сплавы 2, 4 и 5 сначала затвердевают в зоне выдержки. Однако к концу затвердевания температурные кривые описывают точку остановки, аналогичную точке остановки чистого металла. Сплав 3 даже затвердевает исключительно в одной точке остановки.
Причина такого поведения кроется в сильном взаимном препятствовании двух компонентов, которые разделяются во время кристаллизации, чтобы иметь возможность образовывать кристаллы своего вида. Максимум взаимной интерференции соответственно у сплава 3, в котором кристаллы компонентов А и В одновременно образуются в точке затвердевания. Однако из-за постоянных взаимных препятствий во время разделения и низкой температуры пути атомов очень малы, и поэтому кристаллическая смесь очень мелкозернистая.
Из-за этой особенности сплав 3 получил название эвтектического сплава (= тонкий ; хорошо сложенный ). Линия солидуса, общая для всех сплавов, называется эвтектической, а соответствующая температура - эвтектической температурой (T Eu ).
Выдающимся примером эвтектического сплава с особенно низкой температурой плавления является сплав Вуда , температура плавления которого составляет 70 ° C.
В сплавах, которые находятся либо слева (= заэвтектика), либо справа (= заэвтектика) от эвтектики, первичные кристаллы компонента A или первичные кристаллы компонента B затвердевают первыми. Расчет начинается в точке T Eu , т.е. в точке, где остаточный расплав только что достиг эвтектического состава:
|
|
M Eu = доля остаточного расплава эвтектического состава = доля эвтектики M Pr = доля первичных кристаллов |
Двухкомпонентные системы с ограниченной растворимостью в твердом состоянии.
Сплавы этого типа могут образовывать смешанные кристаллы, но не во всех составах. В отличие от сплавов с полной растворимостью размеры атомов различаются сильнее, а это означает, что искажения решетки становятся невыносимыми от определенного состава. Кристаллическая система также может быть препятствием, если легирующие элементы в кристаллической системе похожи, но не одинаковы.
Например, каждый компонент в сплаве свинец (гранецентрированный кубический) - олово (объемноцентрированный тетрагональный) может образовывать обменные смешанные кристаллы друг с другом в ограниченной степени.
Типичные MC-образующие с ограниченной растворимостью: алюминий-магний, свинец-олово, медь-алюминий, медь-цинк, медь-олово, цинк-алюминий.
Ограниченная растворимость в твердом состоянии означает не только то, что один компонент может абсорбировать до определенного процента атомов из другого компонента во время кристаллизации, но также то, что растворимость уменьшается при понижении температуры. Поскольку кинетическая энергия атомов уменьшается, постоянная решетки существующей кристаллической системы, естественно, также соответственно сокращается , и остается меньше места для посторонних атомов. Следствием этого является то, что смешанные кристаллы начинают отделяться от температуры перехода T Ü .
Именно это свойство - частичная сегрегация компонентов из-за снижения растворимости при более низких температурах - используется при закалке такого сплава. Это также называется дисперсионным твердением .
|
|
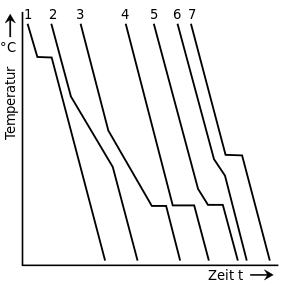
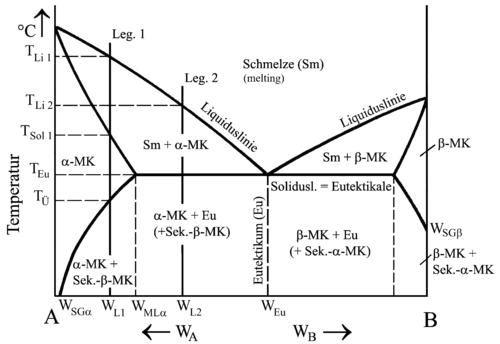
| Кривые охлаждения и фазовая диаграмма сплава различного состава с образованием твердого раствора ограниченной растворимости в твердом состоянии | |
Таким образом, сплав 1 затвердевает от T Li 1 до T Sol 1 с образованием смешанных кристаллов с кристаллической системой A, называемых α-кристаллами. Однородное состояние сохраняется до T Ü . Смешанные кристаллы являются насыщенными, что означает, что компонент A поглотил компонент B до максимальной растворимости для этого сплава.
При T Ü атомы B мигрируют к границам зерен в соответствии с максимальной растворимостью для этой температуры и образуют вторичные смешанные кристаллы с кристаллической системой B, называемые β смешанными кристаллами. Чтобы компенсировать это, атомы A диффундируют внутрь зерна.
Долю вторичных смешанных кристаллов можно рассчитать по следующей формуле:
|
|
M Sβ = доля вторичных β смешанных кристаллов W L = состав сплава W Sα и W Sβ соответствуют при комнатной температуре W SGα и W SGβ (SG = предел насыщения) |
Сплав 2 первоначально кристаллизуется точно так же, как сплав 1. Однако, когда достигается эвтектика, остаточный расплав затвердевает в точке разрыва и образуется мелкозернистая смесь смешанных кристаллов α и β, которая, как и в случае образования отдельных кристаллов, называется эвтектика. Созданные ранее α смешанные кристаллы соответствуют первичным кристаллам.
В этом сплаве атомы B также отделяются от первичных смешанных α-кристаллов ниже эвтектики. Чтобы иметь возможность рассчитать долю вторичных β-смешанных кристаллов из первичных кристаллов, сначала необходимо рассчитать долю первичных кристаллов в общем сплаве. Расчет соответствует расчету для раздельной кристаллизации. Затем рассчитывается доля вторичных β-смешанных кристаллов из первичных кристаллов и умножается на долю первичных кристаллов:
| 1)
2) 3) |
M Pr = доля первичных кристаллов в% W Eu = состав эвтектики |
Расчет пропорций вторичных кристаллов в эвтектике не имеет смысла, потому что они не образуют здесь новую фазу. Только атомы перегруппируются при сохранении кристаллической системы. Поэтому никаких отличий ни на микрофотографии, ни в технических свойствах не обнаружено.
Промежуточные кристаллы
Другая возможность легирования состоит в том, что участвующие элементы образуют общий кристалл, но он не похож ни на одну кристаллическую систему из основных элементов. В результате получается собственная кристаллическая система, которая, в отличие от чистых металлов, может иметь очень сложную структуру. Такие соединения тоже очень твердые и хрупкие. Кроме того, для этих кристаллов требуется фиксированное соотношение атомных номеров. Сплав с промежуточным образованием кристаллов , легирующими элементами которого являются исключительно металлы, называют интерметаллической фазой (с растворимостью составляющих элементов) или интерметаллическим соединением (со стехиометрическим составом). Если такая фаза возникает, на диаграмме плавления может наблюдаться дистектика .
Примерами промежуточной кристаллизации являются Al 2 Cu, Mg 2 Si, Cu 4 Sn, Fe 3 C ( цементит ) и WC ( карбид вольфрама ).
Формула кристаллизации аналогична формуле для химических соединений, которые, в отличие от сплавов, имеют совершенно другой тип соединения .
Классификация по схеме химических веществ
| Схематическая классификация веществ | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Смотри тоже
литература
- Стефан Хассе: Литейный лексикон . Schiele & Schön, Берлин 1997, ISBN 3-7949-0606-3 (Приложение со стр. 1430 с многочисленными диаграммами состояний двойных и тройных систем сплавов).
- А. Ф. Холлеман , Э. Виберг , Н. Виберг : Учебник неорганической химии . 101-е издание. Вальтер де Грюйтер, Берлин, 1995 г., ISBN 3-11-012641-9 .
- Альфред Бёге: Справочник техника . 13-е, переработанное издание. Vieweg, Брауншвейг 1992, ISBN 3-528-14053-4 .
- Эрхард Хорнбоген: Материалы . Springer, Берлин, Гейдельберг, Нью-Йорк, 2006 г., ISBN 3-540-30723-0 .
- Дитер Кохц: Введение в материаловедение для сварщиков металлов . В: Der Praktiker: журнал по сварочной технике и не только . С 9/1982 по 1/1985. ДВС-Верлаг, ISSN 0554-9965 .
- Эрвин Ридель : неорганическая химия . de Gruyter, Берлин, 2002 г., ISBN 3-11-017439-1 .
- Ульрих Мюллер: неорганическая структурная химия . Б. Г. Тойбнер, Штутгарт, 2004 г., ISBN 3-519-33512-3 .
- Вильгельм Домке: Материаловедение и испытания материалов . 10-е издание. Cornelsen, Дюссельдорф, 1987, ISBN 3-590-81220-6 .
веб ссылки
Индивидуальные доказательства
- ↑ Дитер Кохц: Введение в материаловедение для сварщиков металлов - что такое сплав . В: Der Praktiker: журнал по сварочной технике и не только . Лента 1 . ДВС-Верлаг, 1984, ISSN 0554-9965 , с. 4 .
- ↑ Лексикон физики: Сплавы. Spektrum Akademischer Verlag, 1998, доступ к 27 января 2018 .
- ↑ www.fremdwort.de: Сплав .
- ↑ Фридрих Бауман: История литья олова. (Больше не доступны в Интернете.) Архивировано из оригинала марта 2, 2009 ; Проверено 2 апреля 2009 года .
- ↑ http://www.kupfer-institut.de/front_frame/frameset.php3?client=1&lang=1&idcat=27&parent=14 (ссылка недоступна)
- ^ Марианна Шённенбек, Франк Нойман: История цинка. Rheinzink , по состоянию на 26 марта 2018 г. ( полный отчет в электронном виде ).
- ↑ Хельмут Фёлль: История стали. В: Введение Материалы Наука I. Accessed 2 апреля 2009 года .














