Липаза поджелудочной железы
| Липаза поджелудочной железы | ||
|---|---|---|
| Свойства человеческого белка | ||
| Масса / длина первичной конструкции | 449 аминокислот | |
| Кофактор | Колипаза | |
| Идентификатор | ||
| Имя гена | PNLIP | |
| Внешние идентификаторы | ||
| Классификация ферментов | ||
| EC, категория | 3.1.1.3 , липазы | |
| Тип ответа | Гидролиз (расщепление гидролитического эфира) | |
| Субстрат | Три- / диацилглицерин + H 2 O | |
| Продукты | Ди- / моноацилглицерин + жирная кислота | |
| Ортолог | ||
| человек | Домовая мышь | |
| Entrez | 5406 | 69060 |
| Ансамбль | ENSP00000358223 | |
| UniProt | P16233 | Q6P8U6 |
| Refseq (мРНК) | NM_000936 | NM_026925 |
| Refseq (белок) | NP_000927 | NP_081201 |
| Генный локус | Chr 10: 116,55 - 116,57 Мб | Chr 19: 58.67 - 58.68 Мб |
| PubMed поиск | 5406 |
69060
|
Панкреатическая липаза (липаза, PL) является одним из двух ферментов , в тонком кишечнике из млекопитающих , зарегистрированных жиров ( триглицериды расколов). Эта реакция необходима для переваривания жиров ; около 80 процентов триглицеридов из пищи уже расщепляются к тому времени, когда достигают средней двенадцатиперстной кишки. PL принадлежит к группе липаз и вырабатывается поджелудочной железой . Для этой функции требуется кофактор протеина колипаза .
Панкреатическая липаза также отвечает за гидролиз в ретиниловых сложных эфиров с ретинолом и жирных кислот , который позволяет часть витамина А поглощения через пищу (витамин А также подается и поглощается непосредственно в качестве провитамина или ретинола).
Липаза поджелудочной железы является мишенью для лекарственного контроля ожирения. Ингибитор PL орлистат продается с этим показанием с 1998 года .
Применение в медицине
Липаза играет центральную роль в заместительной ферментной терапии в случае нарушения функции поджелудочной железы ( недостаточность поджелудочной железы ). В частности, в случае муковисцидоза стандартным лечением является введение ферментных препаратов с порошком поджелудочной железы от свиней, которые стандартизированы до определенного содержания липазы. Эти препараты предлагаются с энтеросолюбильным покрытием для защиты содержащихся в них ферментов. В некоторых случаях используется липаза из неживотных источников (ризолипаза из плесени Rhizopus oryzae, торговое название: Nortase ), которая характеризуется своей естественной устойчивостью к кислоте желудочного сока человека .
Лабораторная диагностика
В лабораторной диагностике активность липазы из плазмы гепарина или сыворотки крови измеряется для устранения боли в верхней части живота, особенно для диагностики острого панкреатита .
Контрольный диапазон для измерений при 37 ° C (цветовой тест): сыворотка, плазма <60 Ед / л
При остром панкреатите липаза повышается и уже превышает норму 60 Ед / л через 5 часов после появления боли. В большинстве случаев значение превышает 180 Ед / л и остается повышенным в течение трех-шести дней.
В целом метод определения липазы менее стандартизирован и более чувствителен к влияющим факторам, чем амилаза поджелудочной железы . Следовательно, при подозрении на острый панкреатит в медицине в первую очередь определяют панкреатическую амилазу. Липаза в качестве добавки полезна, если по техническим причинам можно измерить только общую амилазу или если пациент лечился с помощью расширителей плазмы (гидроксиэтилкрахмал или декстран 70). С другой стороны, в ветеринарии общая концентрация липазы поджелудочной железы в сыворотке для диагностики острого панкреатита определяется у собак и кошек как иммунореактивность липазы поджелудочной железы .
Липаза фильтруется клубочками в почках, но затем не выводится, а реабсорбируется и расщепляется. Поэтому он не появляется в моче , но, тем не менее, увеличивается в случае почечной недостаточности.
Во время эндоскопического исследования поджелудочной железы ( ЭРХПГ = эндоскопическая ретроградная холангиопанкреатография) липаза немедленно увеличивается, достигает значений до 720 Ед / л через шесть часов и остается выше референсного диапазона 60 Ед / л до трех дней. .
Другой причиной повышения липазы без заболевания может быть синдром Гулло .
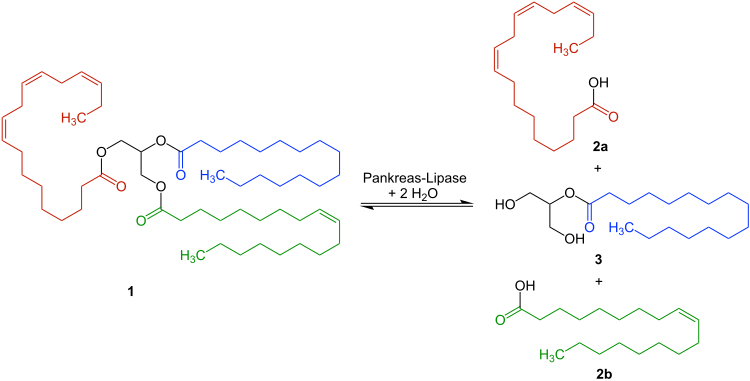
Катализированная реакция
Липаза поджелудочной железы расщепляет триглицериды - например, Б. 1 - только остатки α-жирных кислот из. Образуются свободные жирные кислоты 2a и 2b, а также моноглицерид 3 :
Механизм реакции
В активном центре липазы находится каталитическая триада, состоящая из аминокислот аспарагиновой кислоты , гистидина и серина . Аспарагиновая кислота удаляет протон из гистидина и, таким образом, активирует его. Каталитически активный гистидин, в свою очередь, удаляет протон из серина , что увеличивает нуклеофильность серинового остатка. Теперь он может атаковать карбонильный углерод сложного эфира субстрата, который уже находится в активном центре. Образуется тетраэдрический промежуточный продукт, из которого образуется комплекс ацил- фермент. Деацетилирование на стадии гидролиза высвобождает жирную кислоту продукта и исходный фермент .
Смотри тоже
литература
- Биргид Ноймейстер, Инго Безенталь, Хартмут Либих (ред.): Клинические рекомендации по лабораторной диагностике. 3. Издание. Урбан и Фишер, Мюнхен и др., 2003 г., ISBN 3-437-22231-7 .
- Лотар Томас (Ред.): Лаборатория и диагностика. Индикация и оценка результатов лабораторных исследований для медицинской диагностики. 6-е издание. TH-Books, Франкфурт-на-Майне 2005, ISBN 3-9805215-5-9 .
веб ссылки
- Липаза на med4you.at
- Стабильность образцов крови, опубликованная ВОЗ (pdf) (292 kB)
- D'Eustachio / reactome.org: Расщепление триацилглицеринов внеклеточными PTL: колипазой
- D'Eustachio / reactome.org: Расщепление диацилглицеринов внеклеточными PTL: колипазой
Индивидуальные доказательства
- ↑ UniProt P16233
- ↑ AM van Bennekum, EA Fisher, WS Blaner, EH Harrison: Гидролиз ретиниловых эфиров триглицерид липазой поджелудочной железы . В кн . : Биохимия . Vol. 39, No. 16, April 2000, pp. 4900-4906. PMID 10769148 .
- ↑ Росс С. Смит, Джеймс Саутвелл-Кили, Дуглас Чешер: Должна ли сывороточная липаза поджелудочной железы заменять сывороточную амилазу в качестве биомаркера острого панкреатита? . В: Журнал хирургии ANZ . Том 75, № 6, июнь 2005 г., стр. 399-404. DOI : 10.1111 / j.1445-2197.2005.03391.x . PMID 15943725 .
- ↑ Йорг М. Штайнер (Ред.): Гастроэнтерология мелких животных. Schlütersche, Ганновер 2008, ISBN 978-3-89993-027-6 .
- ^ Otto-Albrecht Ноймюллер (редактор): Römpps Chemie Lexikon , Frank'sche Verlagshandlung, Stuttgart, 1983, 8 - е издание, стр 2377,. ISBN 3-440-04513-7 .
- ^ Питер Нун: Naturstoffchemie , S. Hirzel Wissenschaftliche Verlagsgesellschaft, Штутгарт, 2-е издание, 1990, стр. 308–309, ISBN 3-7776-0473-9 .