Ванадий
| характеристики | ||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| В целом | ||||||||||||||||||||||||||||||||||
| Имя , символ , атомный номер | Ванадий, В, 23 | |||||||||||||||||||||||||||||||||
| Категория элемента | Переходные металлы | |||||||||||||||||||||||||||||||||
| Группа , период , блок | 5 , 4 , д | |||||||||||||||||||||||||||||||||
| Посмотрите | стальной серый металлик, мерцающий голубоватый | |||||||||||||||||||||||||||||||||
| Количество CAS | 7440-62-2 | |||||||||||||||||||||||||||||||||
| Номер ЕС | 231-171-1 | |||||||||||||||||||||||||||||||||
| ECHA InfoCard | 100.028.337 | |||||||||||||||||||||||||||||||||
| Массовая доля земной оболочки | 0,041% | |||||||||||||||||||||||||||||||||
| Атомный | ||||||||||||||||||||||||||||||||||
| Атомная масса | 50.9415 (1) и | |||||||||||||||||||||||||||||||||
| Атомный радиус (рассчитанный) | 135 (171) вечера | |||||||||||||||||||||||||||||||||
| Ковалентный радиус | 153 вечера | |||||||||||||||||||||||||||||||||
| Электронная конфигурация | [ Ar ] 3 д 3 4 с 2 | |||||||||||||||||||||||||||||||||
| 1. Энергия ионизации | 6-е.746 187 (21) эВ ≈ 650.91 кДж / моль | |||||||||||||||||||||||||||||||||
| 2. Энергия ионизации | 14-е.634 (7) эВ ≈ 1 412 кДж / моль | |||||||||||||||||||||||||||||||||
| 3. Энергия ионизации | 29.3111 (25) эВ ≈ 2 828.09 кДж / моль | |||||||||||||||||||||||||||||||||
| 4. Энергия ионизации | 46.709 (5) эВ ≈ 4 506.7 кДж / моль | |||||||||||||||||||||||||||||||||
| 5. Энергия ионизации | 65.28165 (17) эВ ≈ 6 298.72 кДж / моль | |||||||||||||||||||||||||||||||||
| Физически | ||||||||||||||||||||||||||||||||||
| Физическое состояние | твердо | |||||||||||||||||||||||||||||||||
| Кристальная структура | объемно-центрированная кубическая | |||||||||||||||||||||||||||||||||
| плотность | 6,11 г / см 3 (20 ° С ) | |||||||||||||||||||||||||||||||||
| Твердость по шкале Мооса | 7.0 | |||||||||||||||||||||||||||||||||
| магнетизм | парамагнитный ( Χ m = 3,8 10 −4 ) | |||||||||||||||||||||||||||||||||
| Температура плавления | 2183 К (1910 ° С) | |||||||||||||||||||||||||||||||||
| точка кипения | 3680 К (3407 ° С) | |||||||||||||||||||||||||||||||||
| Молярный объем | 8,32 10 −6 м 3 моль −1 | |||||||||||||||||||||||||||||||||
| Теплота испарения | 444 кДж / моль | |||||||||||||||||||||||||||||||||
| Теплота плавления | 21,5 кДж моль -1 | |||||||||||||||||||||||||||||||||
| Скорость звука | 4560 м с −1 при 293,15 К. | |||||||||||||||||||||||||||||||||
| Удельная теплоемкость | 489 Дж кг −1 K −1 | |||||||||||||||||||||||||||||||||
| Электрическая проводимость | 5 · 10 6 А · В −1 · м −1 | |||||||||||||||||||||||||||||||||
| Теплопроводность | 31 Вт · м −1 · K −1 | |||||||||||||||||||||||||||||||||
| Химически | ||||||||||||||||||||||||||||||||||
| Состояния окисления | +5 , +4, + 3, + 2 | |||||||||||||||||||||||||||||||||
| Электроотрицательность | 1,63 ( шкала Полинга ) | |||||||||||||||||||||||||||||||||
| Изотопы | ||||||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||||||
| Для других изотопов см. Список изотопов | ||||||||||||||||||||||||||||||||||
| ЯМР свойства | ||||||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||||||
| Инструкции по технике безопасности | ||||||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||||||
|
Насколько это возможно и общепринято, используются единицы СИ . Если не указано иное, приведенные данные относятся к стандартным условиям . | ||||||||||||||||||||||||||||||||||
Ванадий , также известный как ванадий , представляет собой химический элемент с символом V и атомным номером 23. Это стально-серый, голубовато-мерцающий переходный металл , очень мягкий в чистом виде . В периодической таблице этот металл вместе с более тяжелым ниобием , танталом и дубнием образует 5-ю группу ИЮПАК или группу ванадия . Большая часть ванадия используется в производстве стали в виде так называемого феррованадия . Добавление ванадия хром - ванадиевой стали увеличивает ударную вязкость , и , таким образом , увеличивает стойкость стали.
Этот элемент имеет разные биологические значения и необходим для многих живых существ . Таким образом , он играет роль в регуляции ферментов в фосфорилирования и используется бактерий к фиксации азота , используемых. С другой стороны, предполагается, что он или его соединения вызывают хромосомные аберрации в качестве мутагенного кластогена и, таким образом, действуют как яд и канцероген .
Наиболее известным соединением ванадия является оксид ванадия (V) , который используется в качестве катализатора для производства серной кислоты .
история
Поздний ванадий был впервые обнаружен в 1801 году испанским минералогом Андресом Мануэлем дель Рио в мексиканской свинцовой руде, позже ванадините . Он назвал новый элемент панхромом из-за множества цветов соединений , а позже - эритронием , потому что соли при подкислении стали красными. Однако дель Рио отменил открытие вскоре после того, как сначала Александр фон Гумбольдт, а затем французский химик HV Collett-Desotils заявили, что новый элемент был загрязнен хромом из-за его сходства с соединениями хрома .
Шведскому химику Нильсу Габриэлю Сефстрёму удалось заново открыть этот элемент в 1830 году . Он исследовал железо из шведского месторождения железной руды Таберг , растворив его в соляной кислоте . При этом он обнаружил, среди других известных веществ, неизвестный элемент, который напоминал хром в некоторых свойствах и уран в других , но не был одним из этих элементов после дальнейших исследований. Он назвал новый элемент в честь Ванадиса , эпитета нордического божества Фрейи . Спустя некоторое время Фридрих Велер , который уже занимался этой задачей в Берцелиусе, представил доказательства идентичности ванадия и эритрония.
Металлический ванадий был впервые в 1867 году Генри Энфилд Роско путем сокращения из ванадия хлорид (II) с водородом производится. Джон Уэсли Марден и Малкольм Рич впервые смогли получить ванадий чистотой 99,7% в 1925 году путем восстановления оксида ванадия (V) кальцием.
Впервые ванадий был использован в 1903 году, когда в Англии была произведена первая ванадийсодержащая сталь . Увеличение использования этого элемента в сталелитейной промышленности началось в 1905 году, когда Генри Форд начал использовать ванадиевую сталь в производстве автомобилей .
Вхождение
Ванадий является обычным элементом на Земле, его доля в континентальной коре составляет около 120 ppm . Цирконий , хлор и хром имеют одинаковое количество элементов . Этот элемент в основном содержится в различных минералах . Несмотря на обилие ванадия, месторождения с высокими концентрациями этого элемента встречаются редко, а многие минералы ванадия встречаются редко. По сравнению с земной корой содержание в морской воде значительно ниже, оно составляет около 1,3 мкг / л.
Наиболее важные минералы ванадия включают, в частности, ванадаты, такие как ванадинит [Pb 5 (VO 4 ) 3 Cl], Descloizit Pb (Zn, Cu) [OH | VO 4 ] и карнотит [K 2 (UO 2 ) 2 (VO 4 ) 2 · 3H 2 O], а также сульфид ванадия Patrónit VS 4 . Большая часть ванадия содержится в следовых количествах в других минералах, особенно в железных рудах, таких как магнетит . Содержание ванадия в титано-магнетитовых рудах обычно составляет от 0,3 до 0,8%, но может достигать 1,7% в некоторых южноафриканских рудах.
Животные и растения содержат ванадий, поэтому в организме человека содержится около 0,3 мг / кг этого элемента. Это в основном расположено в ядрах клеток или митохондриях . Некоторые живые существа, особенно некоторые виды морских брызг и мухоморов , способны обогащать ванадий. Содержание ванадия в морских брызгах до 10 7 раз выше, чем в окружающей морской воде. Из-за содержания ванадия в живых существах уголь и сырая нефть, образующиеся из них, также содержат ванадий. Содержание до 0,1%. Особенно высокое содержание ванадия содержится в нефти Венесуэлы и Канады.
В 2015 году было добыто 79 400 тонн ванадиевой руды (в пересчете на металлический ванадий). Наиболее важными странами-производителями являются Южная Африка , Китай и Россия . При известных запасах в 15 миллионов тонн (по состоянию на 2015 год) узких мест в поставках ванадия в обозримом будущем не ожидается.
→ Категория: Ванадий минеральный
Ванадий как минерал
Ванадий признан минералом Международной минералогической ассоциацией (IMA) с 2012 года . Впервые он был обнаружен Михаилом Остроумовым как продукт повторной сублимации в высокотемпературных фумаролах мексиканского вулкана Колима . Калий ванадия сульфида Colimait (К 3 В. С. 4 ) и оксид ванадия Shcherbinait (V 5+ 2 O 5 ) , которые также были обнаружены там в первый раз, появился в качестве сопровождающих минералов .
Первое описание было опубликовано Остроумовым и Юрием Тараном в 2015 году, первоначально в « Макле». Revista de la Sociedad Española de Mineralogía и 2016 г. в Mineralogical Magazine .
Помимо своего типичного местоположения на вулкане Колима ванадий был достойным, но только в неустановленном Hibonit -Fundstätte в Сьерра-де-лос- Комечингонес в Аргентине . Еще одна находка на карьерном ванадиевом карьере Рован недалеко от Рустенбурга в южноафриканской провинции Северо-Запад еще не подтверждена.
Согласно систематике минералов по Струнцу (9-е издание) ванадий классифицируется под номером системы. 1.AF.05 (элементы - металлы и интерметаллиды - семейство железо-хром - группа железа).
Извлечение и представление
Ванадий представлен в несколько ступеней. Прежде всего, оксид ванадия (V) должен быть получен из различных исходных материалов . Затем его можно превратить в элементарный металл и при необходимости очистить.
Возможными исходными материалами, из которых может быть извлечен ванадий, являются ванадиевые руды, такие как карнотит или патронит, ванадийсодержащие титано-магнетитовые руды и нефть . Руды ванадия были важны для производства в прошлом, но больше не играют важной роли и в основном были заменены титаномагнетитовыми рудами.
Если железные руды, содержащие ванадий, восстанавливаются до железа в доменном процессе , ванадий первоначально остается в чугуне . Для дальнейшей переработки чугуна в сталь в процессе рафинирования вдувается кислород. Ванадий переходит в шлак . Он содержит до 25% оксида ванадия (V) и является наиболее важным источником для извлечения металла. Чтобы получить чистый оксид ванадия (V), тонкоизмельченный шлак обжигают окислительным способом с помощью солей натрия, таких как хлорид натрия или карбонат натрия . В процессе образуется водорастворимый метаванадат натрия , который отделяется от оставшегося шлака выщелачиванием. Образовавшийся нерастворимый поливанадат аммония выпадает в осадок из раствора при добавлении кислоты и солей аммония . Его можно превратить в оксид ванадия (V) путем обжига . Оксид также может быть получен из других ванадийсодержащих руд аналогичным способом. Ванадий может быть извлечен из нефти путем образования эмульсии с добавлением воды и нитрата магния . Дальнейшая переработка происходит так же, как при добыче из железной руды.
Фактическое извлечение ванадия происходит путем восстановления оксида ванадия (V) другими металлами. В качестве восстановителей можно использовать алюминий , кальций , ферросилиций или углерод ; с последним, однако, в реакции образуются карбиды , которые трудно отделить от металла.
- Восстановление кальцием
Для получения чистого ванадия в качестве восстановителя используется дорогой кальций или алюминий , поскольку более дешевый ферросилиций не может обеспечить высокую чистоту. В то время как чистый ванадий получается непосредственно с кальцием, сплав ванадия с алюминием первоначально образуется с алюминием, из которого чистый ванадий получается сублимацией в вакууме .
Большая часть ванадия используется не как чистый металл, а в виде феррованадия из сплава железо-ванадий , который содержит не менее 50% ванадия. Для этого нет необходимости заранее извлекать чистый ванадий. Вместо этого ванадий и железосодержащий шлак восстанавливают до феррованадия с помощью феррокремния и извести . Этого сплава достаточно для большинства технических применений.
Чистейший ванадий может быть получен электрохимическим способом или методом Ван-Аркеля-де-Бура . Для этого чистый ванадий плавят вместе с йодом в пустой стеклянной ампуле. Иодид ванадия (III), образующийся в нагретой ампуле, разлагается на горячей вольфрамовой проволоке с образованием ванадия и йода высокой чистоты.
- Реакция в процессе Ван Аркеля де Бура
характеристики
Физические свойства
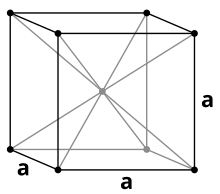
Ванадий - немагнитный, прочный, ковкий тяжелый металл синего цвета с плотностью 6,11 г / см 3 . Чистый ванадий относительно мягкий, но становится тверже при добавлении других элементов, и тогда он обладает высокой механической прочностью. По большинству свойств он похож на своего соседа по таблице Менделеева - титан . Температура плавления чистого ванадия составляет 1910 ° C, но она значительно увеличивается из- за примесей, таких как углерод . При содержании углерода 10% это около 2700 ° C. Ванадий кристаллизуется подобно хрому или ниобию в объемно-центрированной кубической кристаллической структуре с пространственной группой Im 3 m (пространственная группа № 229) и параметром решетки a = 302,4 пм, а также двумя формульными единицами на элементарную ячейку .
Ниже критической температуры 5,13 К ванадий становится сверхпроводником . Как и чистый ванадий, сплавы ванадия с галлием , ниобием и цирконием являются сверхпроводящими. При температурах ниже 5,13 К ванадий, как и металлы ванадиевой группы ниобий и тантал , проявляет крошечными кусочками до 200 атомов спонтанную электрическую поляризацию, которая еще не была объяснена, которая иначе проявляется только неметаллическими веществами .
Химические свойства
Ванадий является неблагородным металлом и может реагировать со многими неметаллами . В воздухе он неделями остается блестящим металлическим. Если смотреть в течение длительного периода времени, видна отчетливо видимая зеленая ржавчина. Если требуется консервация ванадия, его следует хранить в атмосфере аргона. В жару он подвергается действию кислорода и окисляется до оксида ванадия (V) . В то время как углерод и азот реагируют с ванадием только в раскаленном состоянии , реакция с фтором и хлором происходит на холоде.
По сравнению с кислотами и основаниями ванадий обычно стабилен при комнатной температуре из-за тонкого пассивирующего оксидного слоя; В этом состоянии он подвергается воздействию только фтористоводородной кислоты и сильно окисляющих кислот, таких как горячая азотная кислота , концентрированная серная кислота и царская водка .
Вплоть до температуры 500 ° С ванадием способен водородом к поглощению . Металл становится хрупким и легко измельчается. Водород можно удалить при 700 ° C в вакууме.
Изотопы
Всего известно 27 изотопов и еще 6 основных изомеров ванадия . Два из них происходят естественным путем. Это изотопы 50 В с собственной частотой 0,25% и 51 В с частотой 99,75%. 50 В слабо радиоактивны , с периодом полураспада 1,5 · 10 17 лет она затухает до 83% с захватом электронов до 50 Ti, 17% с бета - распада до 50 Cr. Оба ядра можно использовать для исследований с помощью ЯМР-спектроскопии .
Наиболее стабильными искусственными изотопами являются 48 В с периодом полураспада 16 дней и 49 В с периодом полураспада 330 дней. Они используются как индикаторы . Все остальные изотопы и изомеры ядра очень нестабильны и распадаются за минуты или секунды.
использовать
Лишь небольшой процент чистого ванадия используется в качестве материала оболочки для ядерного топлива из-за его малого сечения захвата нейтронов . Однако также можно использовать более стойкие ванадиевые сплавы. Более 90% продукции используется в различных сплавах , в основном с железом, титаном, никелем, хромом, алюминием или марганцем. Лишь небольшая часть используется в соединениях, в основном в виде оксида ванадия (V).
Поскольку 85% произведенного ванадия, подавляющее большинство его потребляется в сталелитейной промышленности . Поскольку для этого не требуется высокая чистота, в качестве сырья используется феррованадий. Даже в небольших количествах ванадий увеличивает прочность и ударную вязкость сталей, а значит, и их износостойкость . Это вызвано образованием твердого карбида ванадия . В зависимости от применения добавляется разное количество ванадия; конструкционные стали и инструментальные стали содержат лишь небольшое количество (от 0,2 до 0,5%) ванадия, быстрорежущие стали - до 5%. Стали, содержащие ванадий, в основном используются для изготовления инструментов и пружин, подверженных механическим нагрузкам.
Титановые сплавы, содержащие ванадий и в основном алюминий, отличаются особой стабильностью и жаропрочностью и используются в авиастроении для изготовления несущих частей и лопаток турбин авиационных двигателей.
Соединения ванадия могут использоваться для электрохимического накопления энергии в проточных окислительно-восстановительных ячейках , см. Ванадиевый окислительно-восстановительный аккумулятор . В этом применении соли ванадия используются в кислых водных растворах, которые можно хранить в резервуарах.
доказательство
Предварительная выборка обеспечивается соль фосфора жемчуг , в котором ванадий появляется характерный зеленый цвета в восстановительном пламени. В пламени окисления бледно - желтый цвет и , следовательно , Неконкретные.
Качественные доказательства ванадия основаны на образовании ионов пероксованадия. Для этого в кислый раствор, содержащий ванадий в степени окисления +5, добавляют немного перекиси водорода . Образуется красновато-коричневый катион [V (O 2 )] 3+ . Он реагирует с большим количеством перекиси водорода с образованием бледно-желтой пероксованадовой кислоты H 3 [VO 2 (O 2 ) 2 ].
Количественно ванадий можно определить титрованием . Для этого раствор серной кислоты, содержащий ванадий, окисляют перманганатом калия до пятивалентного ванадия, а затем повторно титруют раствором сульфата железа (II) и дифениламином в качестве индикатора . Также возможно восстановление пятивалентного ванадия, присутствующего с сульфатом железа (II), до четырехвалентной степени окисления и последующее потенциометрическое титрование раствором перманганата калия.
В современной аналитике ванадий можно обнаружить несколькими методами. Это, например, атомно-абсорбционная спектрометрия при 318,5 нм и спектрофотометрия с N-бензоил-N-фенилгидроксиламином в качестве цветного реагента при 546 нм.
Биологическое значение

Соединения ванадия имеют различное биологическое значение. Для ванадия характерно то, что он присутствует как в анионной форме в виде ванадата, так и в катионной форме в виде VO 2 + , VO 2+ или V 3+ . Ванадаты очень похожи на фосфаты и, соответственно, имеют аналогичные эффекты. Поскольку ванадат сильнее связывается с подходящими ферментами, чем фосфат, он способен блокировать и, таким образом, контролировать ферменты фосфорилирования . Это касается, например, натрий-калий-АТФазы , которая контролирует транспорт натрия и калия в клетки. Это препятствие можно быстро удалить с помощью десфериоксамина B , который образует стабильный комплекс с ванадатом. Ванадий также влияет на усвоение глюкозы . Он способен стимулировать гликолиз в печени и подавлять конкурентный процесс глюконеогенеза . Это снижает уровень глюкозы в крови. Поэтому изучается, подходят ли соединения ванадия для лечения сахарного диабета 2 типа . Однако четких результатов пока нет. Ванадий также стимулирует окисление фосфолипидов и подавляет синтез холестерина , ингибируя скваленсинтазу , микросомальную ферментную систему в печени. Следовательно, дефицит вызывает повышение уровня холестерина и триглицеридов в плазме крови .
Ванадий играет роль в фотосинтезе растений . Он способен катализировать реакцию с образованием 5-аминолевулиновой кислоты без фермента. Это важный предшественник образования хлорофилла .
В некоторых организмах присутствуют ванадийсодержащие ферменты, например, у некоторых видов бактерий есть ванадийсодержащие нитрогеназы для фиксации азота . Это, например, виды рода Azotobacter и цианобактерии Anabaena variabilis . Однако эти нитрогеназы не так эффективны, как более распространенные нитрогеназы молибдена, и поэтому активируются только при дефиците молибдена. Другие ферменты, содержащие ванадий, можно найти в бурых водорослях и лишайниках . В них есть ванадийсодержащие галопероксидазы, с которыми они образуют хлорорганические, бромные или йодорганические соединения.
Функция ванадия, который присутствует в больших количествах в морских брызгах как металлопротеин ванабин , пока не известна. Первоначально предполагалось, что ванадий, как и гемоглобин, служит переносчиком кислорода; однако было обнаружено, что это неверно.
Опасности
Как и другие металлические частицы, ванадиевая пыль легко воспламеняется. В экспериментах на животных было показано, что ванадий и его неорганические соединения обладают канцерогенными свойствами . Поэтому они относятся к категории канцерогенов 2. При длительном вдыхании ванадиевой пыли работниками плавки металлов может возникнуть так называемый ванадизм . Это признанное профессиональное заболевание может проявляться раздражением слизистых оболочек , изменением цвета языка на черный и зеленый, а также хроническими заболеваниями бронхов, легких и кишечника.
ссылки
Ванадий может присутствовать в соединениях в различных степенях окисления . Часто уровни +5, +4, +3 и +2, реже +1, 0, -1 и -3. Наиболее важные и наиболее стабильные степени окисления - +5 и +4.
→ Категория: Соединение ванадия
Водный раствор
Ванадий легко превращается в водный раствор в различные степени окисления. Поскольку разные ионы ванадия имеют характерный цвет, цвет меняется.
В кислом растворе пятивалентный ванадий образует бесцветные ионы VO 2 + , которые при восстановлении до голубого цвета являются ионами первого четырехвалентного VO 2+ . Трехвалентный уровень с ионами V 3+ - зеленый, самый глубокий уровень, который может быть достигнут в водном растворе, двухвалентный ион V 2+ - серо-фиолетовый.
Кислородные соединения
Наиболее важным и наиболее стабильным ванадий-кислородным соединением является оксид ванадия (V) V 2 O 5 . Это соединение оранжевого цвета используется в больших количествах в качестве катализатора для производства серной кислоты. Там он действует как переносчик кислорода и во время реакции восстанавливается до другого оксида ванадия, оксида ванадия (IV) VO 2 . Другими известными оксидами ванадия являются оксид ванадия (III) V 2 O 3 и оксид ванадия (II) VO.
В щелочном растворе оксид ванадия (V) образует ванадаты , соли с анионом VO 4 3– . Однако в отличие от аналогичных фосфатов ион ванадата является наиболее стабильной формой; Водород и дигидрованадаты, а также свободная ванадиевая кислота нестабильны и известны только в разбавленных водных растворах. При подкислении основных ванадатных растворов вместо гидрованадатов образуются поливанадаты, в которых накапливается до десяти ванадатных звеньев. Ванадаты могут быть найдены в различных минералах, примерами являются ванадинит , десклоицит и карнотит .
Галогенные соединения
Ванадий образует большое количество соединений с галогенами фтором , хлором , бромом и йодом . В степенях окисления +4, +3 и +2 есть соединения со всеми галогенами, только с йодом известны соединения в состояниях +2 и +3. Из этих галогенидов, однако, только хлориды ванадия (IV) , хлорид и ванадия хлорид (III) , являются технически актуальными. Помимо прочего, они служат катализатором производства этилен-пропилен-диенового каучука .
Хлориды оксида ванадия
Ванадий также образует смешанные соли с кислородом и хлором, так называемые хлориды оксида ванадия . Оксихлорид ванадия (III) , VOCl, представляет собой водорастворимый порошок желто-коричневого цвета. Оксихлорид ванадия (IV) , VOCl 2 , используемый в фотографии и в качестве красителя для ткани, состоит из зеленых гигроскопичных кристаллических таблеток, которые растворяются в воде и имеют синий цвет. Наконец, оксихлорид ванадия (V) , VOCl 3 , представляет собой жидкость желтого цвета, которая очень легко гидролизуется водой . VOCl 3 используется в качестве компонента катализатора при полимеризации этилена при низком давлении.
Больше соединений ванадия
В органических соединениях ванадия ванадий достигает своей низшей степени окисления 0, -I и -III. Особое значение здесь имеют металлоцены , так называемые ванадоцены . Они используются в качестве катализаторов для полимеризации из алкинов .
Карбид ванадия VC используется, в частности, в виде порошка для плазменного напыления или плазменной наплавки . Кроме того, карбид ванадия добавляют к твердым металлам , чтобы уменьшить рост зерен .
литература
- Гюнтер Бауэр, в том числе: ванадий и соединения ванадия. В: Энциклопедия промышленной химии Ульмана . Wiley-VCH, Weinheim 2000, DOI : 10.1002 / 14356007.a27_367 .
- Норман Н. Гринвуд, Алан Эрншоу: химия элементов. 1-е издание. VCH, Weinheim 1988, ISBN 3-527-26169-9 .
- А. Ф. Холлеман , Э. Виберг , Н. Виберг : Учебник неорганической химии . 102-е издание. Вальтер де Грюйтер, Берлин 2007, ISBN 978-3-11-017770-1 , стр. 1542–1552.
веб ссылки
- Вход в ванадий. В: Römpp Online . Георг Тиме Верлаг, по состоянию на 25 декабря 2014 г.
Индивидуальные доказательства
- ↑ а б Гарри Х. Биндер: Словарь химических элементов. С. Хирцель Верлаг, Штутгарт 1999, ISBN 3-7776-0736-3 .
- ↑ Значения свойств (информационное окно) взяты с www.webelements.com (vanadium) , если не указано иное .
- ↑ CIAAW, Standard Atomic Weights Revised 2013 .
- ↑ б с д е запись на ванадий в Kramida, A., Ральченко, Ю., Reader, J. и NIST ASD Team (2019):. NIST Атомные спектры базы данных (версия 5.7.1.) . Издание: НИСТ , Гейтерсбург, Мэриленд. DOI : 10.18434 / T4W30F ( https://physics.nist.gov/asd ). Проверено 11 июня 2020 года.
- ↑ б с д е входа на ванадий в WebElements, https://www.webelements.com , доступ на 11 июня 2020 года.
- ^ Н. Н. Гринвуд, А. Эрншоу: Химия элементов. 1-е издание. VCH, Weinheim 1988, ISBN 3-527-26169-9 , стр. 1260.
- ↑ Роберт К. Уист (ред.): Справочник CRC по химии и физике . CRC (Chemical Rubber Publishing Company), Boca Raton 1990, ISBN 0-8493-0470-9 , стр. E-129 - E-145. Значения здесь основаны на г / моль и даны в единицах cgs. Приведенное здесь значение представляет собой рассчитанное на его основе значение в системе СИ без единицы измерения.
- ↑ a b Иминь Чжан, Джулиан Р.Г. Эванс, Шоуфэн Ян: Скорректированные значения точек кипения и энтальпий испарения элементов в справочниках. В: Journal of Chemical & Engineering Data. 56, 2011, стр. 328-337, DOI : 10.1021 / je1011086 .
- ↑ Дэвид Р. Лид (Ред.): Справочник CRC по химии и физике . 90-е издание. (Интернет-версия: 2010 г.), CRC Press / Taylor and Francis, Boca Raton, FL, Fluid Properties; Энтальпия плавления , стр. 6-135.
- ↑ запись на ванадий, порошок в базе вещества GESTIS из на выставке IFA , доступ к 30 апреля 2017 года. (Требуется JavaScript)
- ↑ Хуан Дж. Родригес-Меркадо, Родриго А. Матеос-Нава, Марио А. Альтамирано-Лозано: Индукция повреждения ДНК в клетках человека, подвергшихся воздействию оксидов ванадия in vitro. В кн . : Токсикология in vitro. 25, No. 8, 2011, pp. 1996-2002, DOI: 10.1016 / j.tiv.2011.07.009 .
- ^ LR Caswell: Андрес дель Рио, Александр фон Гумбольдт и дважды обнаруженный элемент. (PDF; 124 кБ). В кн .: Изв. Chem. 28 (1), 2003, стр. 35-41.
- ↑ Н.Г. Сефстём: О ванадии , новом металле, обнаруженном в катанке на Экерсхольме, металлургическом заводе, который получает руду из Таберга в Смоланде. В: Аннал. d. Физика . 97 (1), 1831, стр. 1-4.
- ↑ «В древности на крайнем севере жила богиня Ванадис, красивая и привлекательная. Однажды в дверь постучали. Богиня села поудобнее и подумала: мог быть еще один стук, но стука больше не было, вместо этого стук пошел вниз по лестнице. Богине было любопытно […] О! [...] это Шалк Велер. [...] Через несколько дней в дверь снова постучали; но удары происходили снова и снова. Наконец богиня пришла сама и открыла дверь. Вошел Сефстрём, и от этой встречи родился Ванадин ». ( Письмо Берцелиуса Веллеру от 22 января 1831 г. В: О. Валлах (Ред.): Переписка между Й. Берцелиусом и Ф. Велером . Лейпциг, 1901. )
- ↑ ванадий. В: Британская энциклопедия. 2008. Encyclopædia Britannica Online, по состоянию на 6 октября 2008 г. (онлайн)
- ↑ б с д е е г ч я J Гюнтер Бауэр и др: Ванадий и ванадиевых соединений. В: Энциклопедия промышленной химии Ульмана. Wiley-VCH, Weinheim 2000, DOI : 10.1002 / 14356007.a27_367 .
- ↑ a b c d Дитер Редер: Биоинорганическая химия ванадия. В: Angew. Chem. , 103, 1991, стр. 152-172.
- ↑ a b c d e f Запись по ванадию. В: Römpp Online . Георг Тиме Верлаг, по состоянию на 25 декабря 2014 г.
- ^ А. Ф. Holleman , Е. Wiberg , Н. Wiberg : Учебник неорганической химии . 102-е издание. Вальтер де Грюйтер, Берлин 2007, ISBN 978-3-11-017770-1 , стр. 1542.
- ↑ a b c А. Ф. Холлеман , Э. Виберг , Н. Виберг : Учебник неорганической химии . 102-е издание. Вальтер де Грюйтер, Берлин 2007, ISBN 978-3-11-017770-1 , стр. 1543.
- ^ Геологическая служба США: Ванадий. В: Сводки по минеральным сырьевым товарам. Январь 2008 г. (PDF; 84 kB).
- ^ PA Williams, F. Hatert, M. Pasero, SJ Mills: Информационный бюллетень IMA / CNMNC 14: Новые минералы и модификации номенклатуры, одобренные в 2012 и 2013 годах . В кн . : Минералогический журнал . Лента 77 , нет. 1 , 2013, с. 1–12 ( main.jp [PDF; 125 кБ ; по состоянию на 1 января 2018 г.]).
- ↑ Михаил Остроумов, Юрий Таран: Открытие самородного ванадия, нового минерала вулкана Колима, штат Колима (Мексика) . В: Макла. Revista de la Sociedad Española de Mineralogía . Лента 20 июля 2015 г., стр. 109–110 ( ehu.eus [PDF; 134 кБ ; по состоянию на 1 января 2018 г.]).
- ↑ Михаил Остроумов, Юрий Таран: Ванадий, V - новый природный минерал из вулкана Колима, штат Колима, Мексика, и его значение для состава фумарольного газа . В кн . : Минералогический журнал . Лента 80 , нет. 2 , апрель 2016 г., стр. 371-382 , DOI : 10,1180 / minmag.2016.080.006 (доступ через De Gruyter Online).
- ↑ Миндат - Ванадий (англ.)
- ↑ Mineralienatlas : Систематика Strunz 9: железо-хромовое семейство
- ↑ К. Шуберт: Модель кристаллической структуры химических элементов. В: Acta Crystallographica . 30, 1974, стр. 193-204, DOI : 10.1107 / S0567740874002469 .
- ^ Аарон Вакслер, Уильям С. Корак: Сверхпроводимость ванадия. В: Физическое обозрение. 85, (1), 1952, стр. 85-90, DOI: 10.1103 / PhysRev . 85.85 .
- ↑ Т. Кроум: Металлы на ложном пути. О необычном низкотемпературном поведении крошечных кусков металла. В: Spektrumdirekt.de. 22 мая 2003 г .; Аннотация .
- ↑ Рамиро Моро, Сяошань Сюй, Шуанье Инь, Уолт А. де Хеер: Сегнетоэлектричество в свободных кластерах ниобия. В кн . : Наука . Том 300, № 5623, 2003 г., стр. 1265-1269, DOI: 10.1126 / science.1083247 .
- ↑ a b G. Audi, FG Kondev, Meng Wang, WJ Huang, S. Naimi: Оценка ядерных свойств NUBASE2016. В: китайской физики С. 41, 2017 г., С. 030001, DOI : 10,1088 / 1674-1137 / 41/3/030001 ( полный текст ).
- ↑ ванадий. В кн . : Лексикон физики. Проверено 9 июля 2008 года.
- ^ A b G. Jander, E. Blasius, J. Strähle: Введение в практический курс неорганической химии. 14-е издание. С. Хирцель Верлаг, Штутгарт 1995, ISBN 3-7776-0672-3 , стр. 218-219.
- ^ DM Smith, RM Pickering, GT Lewith: систематический обзор пероральных добавок ванадия для гликемического контроля при сахарном диабете 2 типа. В: QJM: Международный медицинский журнал . 101, (5), 2008, стр. 351-358, DOI: 10.1093 / qjmed / hcn003 .
- ↑ ванадий. В кн . : Лексикон биологии. Проверено 9 июля 2008 года.
- ^ A b Вольфганг Кайм, Бриджит Шведерски : Bioinorganische Chemie. 4-е издание. Teubner, Wiesbaden 2005, ISBN 3-519-33505-0 , стр. 241-243.
- ↑ Пресс-релиз DFG об изменениях в списке значений MAK и BET ( памятная записка от 13 августа 2007 г. в Интернет-архиве ), 19 июля 2005 г.
- ↑ Хлорид оксида ванадия. В: Лексикон химии. Проверено 9 июля 2008 года.
- ↑ Введение по органическим соединениям ванадия. В: Römpp Online . Георг Тиме Верлаг, по состоянию на 25 декабря 2014 г.
- ↑ Использование карбида ванадия от HC Starck Group.