Хлоруксусная кислота
| Структурная формула | |||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
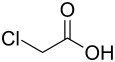
| |||||||||||||||||||
| Общий | |||||||||||||||||||
| Фамилия | Хлоруксусная кислота | ||||||||||||||||||
| Другие названия | |||||||||||||||||||
| Молекулярная формула | С 2 Н 3 ClO 2 | ||||||||||||||||||
| Краткое описание |
бесцветное твердое вещество с резким запахом |
||||||||||||||||||
| Внешние идентификаторы / базы данных | |||||||||||||||||||
| |||||||||||||||||||
| характеристики | |||||||||||||||||||
| Молярная масса | 94,50 г моль -1 | ||||||||||||||||||
| Физическое состояние |
твердо |
||||||||||||||||||
| плотность |
1,58 г см −3 (20 ° С) |
||||||||||||||||||
| Температура плавления |
61 ° С |
||||||||||||||||||
| точка кипения |
189 ° С |
||||||||||||||||||
| Давление газа |
2,14 Па (20 ° C) |
||||||||||||||||||
| значение pK s |
2,87 (25 ° С) |
||||||||||||||||||
| растворимость |
очень хорошо в воде (4210 г л -1 при 20 ° С) |
||||||||||||||||||
| Инструкции по технике безопасности | |||||||||||||||||||
| |||||||||||||||||||
| Термодинамические свойства | |||||||||||||||||||
| ΔH f 0 |
-509,7 кДж / моль |
||||||||||||||||||
| Насколько это возможно и общепринято, используются единицы СИ . Если не указано иное, приведенные данные относятся к стандартным условиям . | |||||||||||||||||||
В хлоруксусных кислотах (также: монохлоруксусная кислота ) а атом водорода в метильную группе из уксусной кислоты была заменена хлором атомом.
презентация
Приготовление происходит путем хлорирования уксусной кислоты при 85 ° C и давлении до 6 бар с добавлением каталитических количеств уксусного ангидрида или ацетилхлорида .
характеристики
Хлоруксусная кислота образует бесцветные кристаллы с резким (как у уксусной кислоты) запахом, которые плавятся при температуре от 53 до 63 ° C (в зависимости от модификации) и легко растворяются в воде , а также в этаноле , диэтиловом эфире и других органических растворителях. Водный раствор сильно кислый, намного более кислый, чем уксусная кислота.
Причиной этого является стабилизация аниона довольно электроотрицательным атомом хлора: он обладает электроноакцепторным эффектом и распределяет (делокализует) отрицательный заряд аниона по всей молекуле и стабилизирует анион.
использовать
Хлоруксусная кислота является исходным материалом для карбоксиметилцеллюлозы , меркаптоуксусной кислоты, а также для пестицидов , красителей или фармацевтических препаратов . Монохлоруксусная кислота используется непосредственно при сжигании бородавок (торговое название: ацетокаустин ).
Использование монохлоруксусной и монобромуксусной кислот в качестве дезинфицирующих средств и консервантов в производстве напитков привело к пивному скандалу в Баварии в 1985 году .
опасности
Хлоруксусная кислота и ее пары ядовиты и оказывают очень разъедающее действие на глаза , дыхательные пути и кожу . Вещество легко всасывается через кожу. При попадании на кожу кислоту необходимо немедленно смыть водой. Существует риск отравления, которое, если намочить от 5 до 10% поверхности тела или 80% раствора или более, может привести к смерти.
Смотри тоже
- Дихлоруксусная кислота
- Трихлоруксусная кислота
- Бромуксусная кислота
- Йодуксусная кислота
- Фторуксусная кислота
веб ссылки
Индивидуальные доказательства
- ↑ Запись о ХЛОРАУЦЕТНОЙ КИСЛОТЕ в базе данных CosIng Комиссии ЕС, по состоянию на 24 февраля 2020 г.
- ↑ б с д е е г записи на хлоруксусной кислоте в базе данных GESTIS вещества в IFA , доступ к 10 января 2017 года. (Требуется JavaScript)
- ↑ Регистрационное досье на Хлоруксусную кислоту (раздел давления паров ) в Европейском химическом агентстве (ECHA), по состоянию на 27 июля 2016 г.
- ↑ Дэвид Р. Лид (Ред.): Справочник CRC по химии и физике . 90-е издание. (Интернет-версия: 2010 г.), CRC Press / Taylor and Francis, Boca Raton, FL, Константы диссоциации органических кислот и оснований, стр. 8-42.
- ↑ запись на хлоруксусной кислоты в классификации и маркировки Перечня в Европейское химическое агентство (ECHA), доступ к 1 февраля 2016 г. Производители или поставщики могут расширить гармонизированной системы классификации и маркировки .
- ↑ Дэвид Р. Лид (Ред.): Справочник CRC по химии и физике . 90-е издание. (Интернет-версия: 2010), CRC Press / Тейлор и Фрэнсис, Бока-Ратон, Флорида, Стандартные термодинамические свойства химических веществ, стр. 5-21.
- ↑ Cantonal Office for Food Inspection St.Gallen: 125 лет кантональной лаборатории, юбилейная публикация 1878–2003 гг. ( Памятная записка от 8 января 2006 г. в Интернет-архиве ).
- ↑ Вольфганг Вагеманн: Решено - Новое дезинфицирующее средство для систем CIP . В: Brauindustrie, 2000 (11), стр. 638-640.



