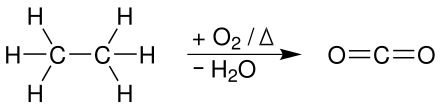Этан
| Структурная формула | ||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
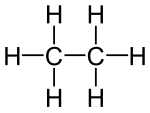
| ||||||||||||||||
| Общий | ||||||||||||||||
| Фамилия | Этан | |||||||||||||||
| Другие названия |
|
|||||||||||||||
| Молекулярная формула | С 2 Н 6 | |||||||||||||||
| Краткое описание |
бесцветный газ без запаха |
|||||||||||||||
| Внешние идентификаторы / базы данных | ||||||||||||||||
| ||||||||||||||||
| характеристики | ||||||||||||||||
| Молярная масса | 30,07 г моль -1 | |||||||||||||||
| Физическое состояние |
газообразный |
|||||||||||||||
| плотность |
|
|||||||||||||||
| Температура плавления |
−183,3 ° С |
|||||||||||||||
| точка кипения |
-88,6 ° С |
|||||||||||||||
| Давление газа |
3,8 МПа (20 ° C) |
|||||||||||||||
| растворимость |
практически не растворим в воде |
|||||||||||||||
| Дипольный момент |
0 |
|||||||||||||||
| Инструкции по технике безопасности | ||||||||||||||||
| ||||||||||||||||
| MAK |
Швейцария: 10 000 мл м -3 или 12 500 мг м -3 |
|||||||||||||||
| Термодинамические свойства | ||||||||||||||||
| ΔH f 0 |
-84,0 кДж / моль |
|||||||||||||||
| Насколько это возможно и обычно, используются единицы СИ . Если не указано иное, приведенные данные относятся к стандартным условиям . | ||||||||||||||||
Этан (на стандартном языке этан ) - химическое соединение , относящееся к алканам (насыщенным углеводородам ). Он имеет эмпирическую формулу C 2 H 6 и представляет собой газ без цвета и запаха, который в основном используется для отопления и сжигания. Этильный радикал (-C 2 H 5 ) является производным от этого . Наряду с метаном этан является основным компонентом природного газа .
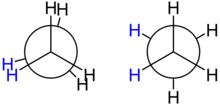
Конформация
У этана две конформации , они различаются своей энергией, которая в данном случае называется энергией кручения , примерно на 12,6 килоджоулей на моль . Он самый высокий в эклиптической конформации и поэтому нестабилен. Он самый низкий в шахматном строении, что, следовательно, является энергетически предпочтительным. Энергия всех других конформаций находится между этими двумя крайностями.
Энергия кручения молекулы этана мала по сравнению с тепловой энергией при комнатной температуре, так что она находится в постоянном вращении вокруг оси CC. Однако он «фиксируется» в шахматной конформации через равные промежутки времени, так что около 99 процентов всех молекул близки к минимуму энергии. Переход между двумя соседними разнесенными конформациями занимает в среднем 10-11 секунд (см. Также конформацию этана ).
характеристики
Этан - газ без цвета и запаха , плавится при -182,76 ° C и кипит при -88,6 ° C. Он плохо растворяется в воде: 61 мг / л при 20 ° C. Для плавления требуется 583 Дж / моль, а для кипячения - 10 кДж / моль.
Твердый этан существует в нескольких модификациях . Когда этан охлаждается при нормальном давлении, создается кубическая кристаллизующаяся форма, в которой молекулы могут вращаться вокруг своей продольной оси, поэтому это пластиковый кристалл . При небольшом дальнейшем охлаждении происходит метастабильная модификация при температуре около 89,9 К, которая кристаллизуется в моноклинной системе.
Критическая температура составляет 32,18 ° С, критическое давление 48,714 бар и критическая плотность 0,2045 г / см.
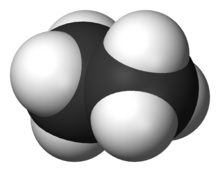
состав
- Длина связки: связка C - C 154 мкм, связка C - H 109 мкм
- Угол соединения : C - H - C: 109,5 °, H - C - H 109,5 ° ( тетраэдрический угол )
Возникновение и представление
| планета | Содержание этана |
|---|---|
| Юпитер | 5,8 ± 1,5 частей на миллион |
| Сатурн | 7 ± 1,5 частей на миллион |
| Нептун | ≈ 1,5 промилле |
Немалые количества этана обнаруживаются в природном газе и болотном газе , но в атмосфере обнаруживаются только его следы. Относительно большое количество метана и этана на Земле в основном связано с их жизненными формами и разложением органических веществ. Но они также возникают без присутствия форм жизни в присутствии водорода и углерода, поскольку представляют собой очень простые соединения.
Следы этана можно найти на планетах Юпитер , Сатурн и Нептун . Этан также обнаружен на некоторых кометах, например, небольшое количество этана было обнаружено в коме кометы Хейла-Боппа . Отложения этана в космосе небольшие и намного меньше метана . Этан также можно найти на некоторых лунах: следы этана можно найти на спутнике Сатурна Энцеладе , 30 июля 2008 года было объявлено, что озеро Онтарио Лак на Титане в основном заполнено этаном. Этанис также можно найти на карликовой планете Плутон .
Он может быть получен в лабораторных масштабах путем Кольбе электролиза из уксусной кислоты или ацетата калия .
опасности
При вдыхании этан вызывает учащенное дыхание и частоту сердечных сокращений. Кроме того, вдыхание в больших количествах приводит к онемению конечностей, бессоннице, спутанности сознания, потере координации и памяти, а также к гипервентиляции. При попадании внутрь вызывает тошноту и рвоту. Поскольку этан обычно хранится в жидкой форме при низких температурах, утечка этана может вызвать обморожение. Этан легко воспламеняется.
Он образует взрывоопасные смеси от 2,7 до 15,5% по объему воздуха, причем наиболее воспламеняющаяся смесь содержит 6,5% по объему этана. Температура вспышки −135 ° C, температура воспламенения 515 ° C.
использовать
Этан сжигается вместе с природным газом для отопления в системах сжигания, его теплотворная способность составляет 64,3 МДж / м³ (47,5 МДж / кг). Он также служит сырьем для синтеза этена , уксусной кислоты и других химических соединений. Этан также используется в качестве хладагента (R 170) в системах охлаждения и кондиционирования воздуха.
Танкеры для перевозки сжиженного газа, такие как Js Ineos Insight , двигатели которых работают на этане, существуют с 2010-х годов .
Реакции
Этан горит с добавлением кислорода с образованием воды и углекислого газа :
Для полного окисления до диоксида углерода требуются идеальные условия реакции (главный критерий: достаточное количество кислорода).
Этан разделяется на водород и этен :
Очень высокая температура (> 700 ° С) необходима для реакции на место.
веб ссылки
- Паспорт безопасности ( памятная записка от 1 февраля 2012 г. в Интернет-архиве ) (PDF; 39 kB)
Индивидуальные доказательства
- ↑ б с д е е г ч я J запись на этана в базе данных вещества GESTIS из в IFA , доступ к 1 февраля 2016 года. (Требуется JavaScript)
- ↑ Дэвид Р. Лид (Ред.): Справочник CRC по химии и физике . 90-е издание. (Интернет-версия: 2010 г.), CRC Press / Тейлор и Фрэнсис, Бока-Ратон, Флорида, Диэлектрическая проницаемость (диэлектрическая проницаемость ) газов, стр. 6-188.
- ↑ запись на этана в классификации и маркировки Перечня в Европейское химическое агентство (ECHA), доступ к 1 февраля 2016 г. Производители или поставщики могут расширить гармонизированной системы классификации и маркировки .
- ↑ Швейцарский фонд страхования от несчастных случаев (Сува): предельные значения - текущие значения MAK и BAT (поиск 74-84-0 или этан ), по состоянию на 15 сентября 2019 г.
- ↑ Дэвид Р. Лид (Ред.): Справочник CRC по химии и физике . 90-е издание. (Интернет-версия: 2010), CRC Press / Тейлор и Фрэнсис, Бока-Ратон, Флорида, Стандартные термодинамические свойства химических веществ, стр. 5-22.
- ↑ GJH van Nes, A. Vos (1978): Монокристаллические структуры и распределение электронной плотности этана, этилена и ацетилена. I. Рентгеноструктурные исследования монокристаллов двух модификаций этана. Acta Cryst. , Разд. B, том 34, стр. 1947-1956 ( DOI: 10.1107 / S0567740878007037 ).
- ↑ Визуализация кристаллической структуры этана как твердого тела .
- ↑ JL Дункан, DC МакКин и AJ Брюс: ИК - спектроскопические исследования частично дейтерированные этаны и г 0 , т г и т е структур . В: Журнал молекулярной спектроскопии . Лента 74 , нет. 3 . Elsevier Inc., март 1979 г., стр. 361-374 , DOI : 10,1016 / 0022-2852 (79) 90160-7 .
- ↑ DLR: спутник Сатурна Титан - ручьи и озера из жидких углеводородов