Гидроксиламин
| Структурная формула | |||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
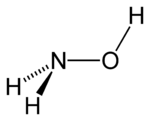
| |||||||||||||||||||
| Клинья для уточнения геометрии | |||||||||||||||||||
| Общий | |||||||||||||||||||
| Фамилия | Гидроксиламин | ||||||||||||||||||
| Другие названия |
Оксиаммоний |
||||||||||||||||||
| Молекулярная формула | NH 2 OH (гидроксиламин) | ||||||||||||||||||
| Краткое описание |
гигроскопичные тромбоциты или иглы без запаха и цвета |
||||||||||||||||||
| Внешние идентификаторы / базы данных | |||||||||||||||||||
| |||||||||||||||||||
| характеристики | |||||||||||||||||||
| Молярная масса | 33,03 г · моль -1 (гидроксиламин) | ||||||||||||||||||
| Физическое состояние |
твердо |
||||||||||||||||||
| плотность |
1,22 г см −3 (14 ° C) |
||||||||||||||||||
| Температура плавления |
|
||||||||||||||||||
| точка кипения |
58 ° C (29 мбар) |
||||||||||||||||||
| Давление газа |
29,33 ч Па (57 ° C, гидроксиламин) |
||||||||||||||||||
| p K S значение |
|
||||||||||||||||||
| растворимость |
|
||||||||||||||||||
| Инструкции по технике безопасности | |||||||||||||||||||
| |||||||||||||||||||
| Насколько это возможно и обычно, используются единицы СИ . Если не указано иное, приведенные данные относятся к стандартным условиям . | |||||||||||||||||||
Гидроксиламин - это бесцветное кристаллическое неорганическое химическое соединение . Соединение термически нестабильно и поэтому продается и используется только в водном растворе.
история
Гидроксиламин был открыт в 1865 году немецким химиком Вильгельмом Лоссеном . Чистое представление было достигнуто в 1891 году голландским химиком Корнелисом Адрианом Лобри ван Троостенбург де Брюн .
синтез
Гидроксиламин может быть получен путем снижения более высокие окислительные уровней из азота ( NO , NO 2 - , NO 3 - ) с водородом , сернистой кислотой или электрическим током . Технически, он производится путем введения смеси монооксида азота и водорода в серной кислоты суспензии в катализаторе ( палладий или платину ) на активированном угле , то выход составляет 90%.
Другой технический прием - введение диоксида серы в раствор нитрита аммония в серной кислоте при температуре от 0 до 5 ° C. В результате образуется диаммонийгидроксиламин бис (сульфонат) N (SO 3 NH 4 ) 2 OH, который медленно расщепляется на гидроксиламин и гидросульфат при 100 ° C с водой . При использовании этого метода выход также составляет около 90%.
Другой технический метод - электрохимическое восстановление азотной кислоты в 50% -ной серной кислоте.
Ответная реакция
Гидроксиламин может храниться несколько недель при исключении доступа воздуха. В водном растворе достаточно устойчив в отсутствие воздуха. В присутствии кислорода воздуха гидроксиламин очень быстро разлагается как в чистом виде, так и в растворе; выше 70 ° C разложение происходит взрывным образом. Но даже концентрированные растворы могут сильно взорваться, как показали аварии в Японии и США.
Из - за его нестабильности, гидроксиламин, в основном , превращают в его соли (например , гидрохлорид гидроксиламина , сульфат гидроксиламмония ).
Относительно высокие температуры плавления и кипения гидроксиламина могут быть перенесены в образование Н-мостика , с другой стороны, путем частичной таутомеризации в оксид амина , что объясняется переносом ионного заряда . Кроме того, гидроксиламин легко действует как амфолит .
Мутагенный эффект
Гидроксиламин превращает цитозин в урацил путем гидролиза . Однако в отличие от цитозина урацил спаривается с аденином, так что пара оснований CG превращается в ТА после двух репликаций . Однако, поскольку урацил не появляется в ДНК , такие ошибки легко выявляются и исправляются.
использовать
Большая часть производимого промышленностью гидроксиламина превращается в оксимы с альдегидами или кетонами . 97% мирового годового производства гидроксиламина используется для получения циклогексаноноксима из циклогексанона , который превращается в полиамид 6 с помощью капролактама (см. Перегруппировку Бекмана ). Он также используется в перегруппировке Небера .
Индивидуальные доказательства
- ↑ Георг Брауэр (ред.), В сотрудничестве с Марианн Бодлер и другими: Справочник по препаративной неорганической химии. 3-е, переработанное издание. Том I, Фердинанд Энке, Штутгарт 1975, ISBN 3-432-02328-6 , стр. 464.
- ↑ a b c Запись о гидроксиламине. В: Römpp Online . Георг Тиме Верлаг, доступ 4 мая 2014 г.
- ↑ б с д е е г записи на гидроксиламине, водный раствор в базе данных GESTIS вещества в IFA , доступ к 10 января 2017 года. (Требуется JavaScript)
- ↑ a b c d e Дэвид Р. Лид (ред.): Справочник CRC по химии и физике . 90-е издание. (Интернет-версия: 2010 г.), CRC Press / Тейлор и Фрэнсис, Бока-Ратон, Флорида, Свойства элементов и неорганических соединений, стр. 4-66.
- ^ Индекс Merck . Энциклопедия химикатов, лекарств и биологических препаратов . 14-е издание, 2006 г., стр. 837, ISBN 978-0-911910-00-1 .
- ^ A b А. Ф. Холлеман , Э. Виберг , Н. Виберг : Учебник неорганической химии . 102-е издание. Вальтер де Грюйтер, Берлин 2007, ISBN 978-3-11-017770-1 .
- ↑ Лист данных гидрохлорид гидроксиламина, 97% от Acros, доступ к 26 сентября 2011 года.
- ↑ Вход на гидроксиламинах (> 55% в водном растворе) в классификации и маркировке Перечне в Европейском химическом агентстве (ECHA), доступ к 1 сентябрю 2016 г. Производители или поставщики могут расширить гармонизированную систему классификации и маркировку .
- ↑ W. Lossen J. Prakt Chem.96 (1865) 462.
- ^ CA Lobry de Bruyn: Sur l'hydroxylamine libre в Recueil des travaux chimiques des Pays-Bas 10 (1891) 100-112.
- ↑ Рольф Вернер Соукуп: Данные химической истории неорганических веществ, версия 2020 г., стр. 36 pdf .
- ↑ М. Бинньюис и другие: Allgemeine und Anorganische Chemie . 2-е издание. Спектр, 2010, ISBN 3-8274-2533-6 . С. 484.
- ↑ Хироши Косэки, Мицуо Кобаяси, Масамицу Тамура: Взрыв и пожар гидроксиламина - город Одзима, Гунма, Япония. В: База данных о сбоях - 100 избранных случаев. Ассоциация по изучению Failure, доступ к 20 апреля 2021 .
- ↑ Взрыв возле Аллентауна, штат Пенсильвания, США .







