Метиловый эфир метакриловой кислоты
| Структурная формула | |||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
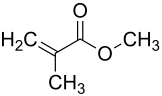
| |||||||||||||||||||
| Общий | |||||||||||||||||||
| Фамилия | Метиловый эфир метакриловой кислоты | ||||||||||||||||||
| Другие названия |
|
||||||||||||||||||
| Молекулярная формула | С 5 Н 8 О 2 | ||||||||||||||||||
| Краткое описание |
бесцветная жидкость с характерным запахом |
||||||||||||||||||
| Внешние идентификаторы / базы данных | |||||||||||||||||||
| |||||||||||||||||||
| характеристики | |||||||||||||||||||
| Молярная масса | 100,12 г моль -1 | ||||||||||||||||||
| Физическое состояние |
жидкость |
||||||||||||||||||
| плотность |
0,94 г см −3 |
||||||||||||||||||
| Температура плавления |
-48,2 ° С |
||||||||||||||||||
| точка кипения |
101 ° С |
||||||||||||||||||
| Давление газа |
|
||||||||||||||||||
| растворимость |
слабо растворим в воде (15 г л -1 при 20 ° C) |
||||||||||||||||||
| Показатель преломления |
1,414 (20 ° С) |
||||||||||||||||||
| Инструкции по технике безопасности | |||||||||||||||||||
| |||||||||||||||||||
| MAK |
DFG / Швейцария: 50 мл м -3 или 210 мг м -3 |
||||||||||||||||||
| Токсикологические данные | |||||||||||||||||||
| Насколько это возможно и общепринято, используются единицы СИ . Если не указано иное, приведенные данные относятся к стандартным условиям . Показатель преломления: линия Na-D , 20 ° C | |||||||||||||||||||
Метиловый эфир метакриловой кислоты ( метилметакрилат , ММА ) представляет собой бесцветную жидкость с неприятным эфирным запахом. ММА легко воспламеняется, легко испаряется и имеет температуру кипения 101 ° C. При смешивании с водой температура кипения ММА падает до 83 ° C с образованием азеотропной смеси. ММА имеет номер ООН 1247.
Производство
ММА в основном производится из циангидрина ацетона , который реагирует с серной кислотой с образованием амида метакриловой кислоты, а затем этерифицируется . Ацетонциангидрин получают из ацетона и цианистого водорода .
Метиловый эфир метакриловой кислоты , также могут быть получены промышленным способом двухстадийного окисления из изобутилена и без использования цианистого водорода. Однако этот так называемый процесс C 4 используется реже. Сам по Изобутен дегидратации из трет - бутанола или путем расщепления метил - трет-бутилового эфира ( МТБЭ производства), оба процесса запуска в газовой фазе, как правило , катализируемой гетерогенным контактами и дают хороший выход изобутилена. Первая стадия окисления приводит к метакролеину , используемые катализаторы аналогичны или получены из контактов, которые также используются для окисления пропена до акролеина.
После производства метиловый эфир метакриловой кислоты стабилизируется во избежание самопроизвольной полимеризации.
Альфа-процесс
Более поздний метод, который был реализован в 2008 году, основан на использовании этилена в качестве сырья, гомогенно катализируемый монооксидом углерода и метанолом в одну стадию карбоксиметилируется, возникает чрезвычайно эффективно с высоким числом оборотов (TOF) и числом оборотов. (TON, мера эффективности катализатора до того, как он будет израсходован побочными реакциями или другими эффектами) метилпропионат в качестве промежуточного продукта. На следующем этапе метилпропионат альдолизируется и обезвоживается в газовой фазе при специальном контакте с формальдегидом , который непосредственно производит ММА. Процесс был первоначально разработан ICI , затем доведен до технической зрелости Lucite International, и, наконец, компания MRC-Lucite в Сингапуре построила производственный объект с годовой производительностью 120 000 тонн. Этот процесс упоминается в литературе как альфа-процесс или альфа-процесс.
Гидроэтерификация этилена оксидом углерода и метанолом до метилпропионата (метилпропионата):
Конденсация метилпропионата и формальдегида до метилметакрилата и воды:
Процесс, который еще не был реализован компанией Lucite (теперь MRC-Lucite) в качестве β-процесса, основан на пропине в качестве исходного материала. Каталитическое превращение пропина с метанолом и оксидом углерода, аналогичное альфа-процессу, используется для преобразования непосредственно в ММА за одну стадию. Несмотря на его высокую каталитическую эффективность, этот процесс еще не применялся, поскольку пропин не является распространенным, продаваемым нефтехимическим сырьем и мало доступен.
LiMA процесс
Последним этапом разработки стал процесс LiMA («Ведущий производитель метакрилатов»), с которым Evonik Industries стала публичной компанией в 2017 году.
Как и альфа-процесс, процесс LiMA также представляет собой процесс C 2, основанный на исходном этилене , при этом этилен гидроформилируется до пропиональдегида в оксосинтезе с синтез-газом на контакте с родием .
На первой стадии ( A ) процесса пропионовый альдегид с LiMA представляет собой формалин HCHO в реакции Манниха с диметиламином / уксусной кислотой - каталисаторгемиш, чтобы прореагировал метакролеин .
Конверсия исходных материалов практически количественная, селективность по метакролеину превышает 98%.
На второй стадии ( B ), метакролеина вступает в реакцию с кислородом воздуха и метанола на никель - золото контакта при низкой температуре (прибл . 90 ° C) и давлении (прибл . 6 бар) , чтобы сформировать метилметакрилат с метакролеина конверсии около 70. % и селективность MMA> 95%.
Пока этот процесс был протестирован только в пилотном масштабе, но он должен быть более рентабельным и экологически безопасным, чем альфа-процесс.
характеристики
Физические свойства
Метиловый эфир метакриловой кислоты представляет собой бесцветную жидкость с температурой плавления -48,2 ° C и температурой кипения 101 ° C при нормальном давлении . Согласно Антуану, функция давления пара получается из log 10 (P) = A− (B / (T + C)) (P в барах, T в K) с A = 5,37785, B = 1945,56 и C = -7,569 дюймов. диапазон температур от 312,4 до 362,3 К. Важные термодинамические параметры приведены в следующей таблице:
| имущество | Тип | Значение [единица] | Замечания |
|---|---|---|---|
| Стандартная энтальпия образования | Δ f H 0 жидкость Δ f H 0 газ |
−388,8 кДж моль −1 −348,7 кДж моль −1 |
как жидкость как газ |
| Энтальпия горения | Δ c H 0 жидкость | −2724,6 кДж моль −1 | как жидкость |
| Теплоемкость | c p | 215,3 Дж моль −1 K −1 (25 ° C) 2,15 Дж г −1 K −1 (25 ° C) |
как жидкость |
| Энтальпия плавления | Δ f H | 13,451 кДж моль -1 | при температуре плавления |
| Энтальпия испарения | Δ V H | 33,3 кДж моль -1 | при температуре кипения при нормальном давлении |
Химические свойства
Метиловый эфир метакриловой кислоты может самопроизвольно полимеризоваться , особенно если он содержит примеси . Из-за эффекта Троммсдорфа происходит резкое повышение температуры, которое сопровождается повышением давления. Эту полимеризацию можно целенаправленно начать путем добавления инициаторов , обычно пероксидов . Теплота полимеризации составляет -59 кДж · моль -1 или -590 кДж · кг -1 .
Параметры безопасности
Метиловый эфир метакриловой кислоты образует легковоспламеняющиеся паровоздушные смеси. Соединение имеет температуру вспышки 10 ° C. Диапазон взрыва составляет от 1,7% по объему (70 г / м 3 ) в качестве нижнего предела взрывоопасности (НПВ) и 12,5% по объему (520 г / м 3 ) в качестве верхнего предела взрывоопасности (ВПВ). Максимальное давление взрыва составляет 8,6 бар. Ограничения зазора ширина была определена в 0,95 мм. Это приводит к отнесению к группе взрывоопасности IIA. Температура возгорания - 430 ° C. Таким образом, вещество относится к температурному классу T2.
использовать
Метиловый эфир метакриловой кислоты в основном используется для производства акрилового стекла . Кроме того, ММА, как правило, является основным компонентом любого пластмассового зубного протеза . Жидкий ММА смешивается с гранулированным ПММА (полиметилметакрилат) до образования вязкого теста и затвердевает (полимеризуется). Однако он также используется в производстве костного цемента для цементирования искусственных швов, в производстве красок и в качестве двухкомпонентного клея ( метилметакрилатного клея ).
Оценка рисков
В 2013 году метиловый эфир метакриловой кислоты был включен в текущий план действий ЕС ( CoRAP ) в соответствии с Регламентом (ЕС) № 1907/2006 (REACH) в рамках оценки вещества . Воздействие вещества на здоровье человека и окружающую среду повторно оценивается и, при необходимости, принимаются последующие меры. Причинами потребления метилметакрилата были опасения по поводу его использования потребителями , воздействия на уязвимые группы населения , высокий (совокупный) тоннаж, высокий коэффициент характеризации риска (RCR) и широкое распространение, а также предполагаемые опасности, связанные с сенсибилизирующими свойствами. Переоценка проводилась с 2014 года во Франции . Затем был опубликован окончательный отчет.
Индивидуальные доказательства
- ↑ вход метилметакрилата в CosIng базе данных Европейской комиссии, доступ к 28 декабря 2020 - ом
- ↑ a b c d e f g h i j k l m n o p q r s t u Запись для № CAS. 80-62-6 в базе вещества GESTIS из в МРС , доступ к 14 марта 2017 года. (Требуется JavaScript)
- ↑ Технический паспорт метилметакрилата от Sigma-Aldrich , по состоянию на 10 апреля 2011 г. ( PDF ).
- ↑ запись на метилметакрилата в классификации и маркировки Перечня в Европейское химическое агентство (ECHA), доступ к 1 августа 2016 г. Производители или дистрибьюторы могут расширить гармонизированной системы классификации и маркировки .
- ↑ Швейцарский фонд страхования от несчастных случаев (Сува): предельные значения - текущие значения MAK и BAT (поиск 80-62-6 или метилметакрилат ), по состоянию на 2 ноября 2015 г.
- ↑ Введение в эфир метакриловой кислоты. В: Römpp Online . Георг Тиме Верлаг, по состоянию на 23 сентября 2014 г.
- ^ Марк В. Хупер: Соображения промышленного тонкого химического синтеза. В: С. М. Робертс, Дж. Сяо, Дж. Уиттолл, Т. Пикетт (ред.): Катализаторы для тонкого химического синтеза. Том 3: Катализируемые металлами реакции образования углерод-углеродных связей. Джон Вили и сыновья, 2004, ISBN 0-470-86199-1 . (PDF)
- ↑ Лучший в своем классе: Evonik разрабатывает наиболее эффективный процесс производства метилметакрилата. В: Пресс-релиз Evonik. Evonik, 5 октября 2017, доступ к 10 июня 2020 .
- ^ Как мы разрабатываем лучший способ получения метилметакрилата. В: Презентация Штеффена Крилла. Evonik, 5 октября 2017, доступ к 10 июня 2020 .
- ↑ Патент WO2014170223A1 : Процесс производства метилметакрилата. Зарегистрировано 11 апреля 2014 г. , опубликовано 23 октября 2014 г. , заявитель: Evonik Industries AG, изобретатели: С. Крилл, Т. Бальдуф, М. Кёстнер, М. Грёмпинг, А. Лыгин, Р. Бургхардт.
- ^ Производство метилметакрилата (ММА) компанией Evonik LiMA ™ Process. В: Обзор PEP. IHS Markit, май 2018, доступ к 10 июня 2020 .
- ↑ Автор: A. Brockhaus, Jenckel, E .: О кинетике термического разложения метилового эфира полиметакриловой кислоты. В кн . : Макромол. Chem. 18, 1956, стр. 262-293, DOI : 10.1002 / macp.1956.020180124 .
- ↑ a b c Р. Вилку, С. Перисану: Энтальпии идеального газового состояния образования некоторых мономеров. В: Преподобный Рум. Чим. 25, 1980, стр. 619-624.
- ↑ М. Карабаев, Т. П. Абдужаминов, А. А. Саидов, Х. Т. Игамбердыев: Теплофизические свойства жидкой метакриловой кислоты и ее простых эфиров. В: Изв. АН Узб. SSR Ser. Физ.-мат. Наук. 4, 1985, с. 71-74.
- ↑ М. Карабаев, А.А. Саидов, Т.П. Абдужаминов, М.М. Кенисарин: Теплоемкость и молекулярно-кинетические процессы конденсированных фаз акрилатов и метакрилатов. В: Изв. АН СССР, сер. Физ.-математика. 6, 1985, стр. 51-54.
- ↑ М.К. Карабаев, Т.П. Абдужаминов, М.М. Кенисарин, А.А. Саидов: Термодинамика фазового перехода кристалл-жидкость в акрилатах и метакрилатах. В: Изв. АН Узб. ССР, сер. Физ.-мат. Наук. 5, 1985, стр. 74-77.
- ↑ Стил В.В., Кирико Р.Д., Коуэлл А.Б., Книпмейер С.Е., А. Нгуен: Термодинамические свойства и энтальпии идеального газа образования транс-метилциннамата, α-метилциннамальдегида, метилметакрилата, 1-нонина, триметилацетилсусной кислоты, триметилацетилсусной кислоты, триметилацетилсульфата. и этилтриметилацетат. В: J. Chem. Eng. Данные . 47, 2002, стр. 700-714, DOI : 10.1021 / je010086r .
- ↑ Ассоциация страхования ответственности работодателей в сырьевой и химической промышленности , буклет R 008 Полиреакции и полимеризуемые системы. Выпуск 05/2015, ISBN 978-3-86825-069-5 , стр. 26.
- ↑ а б в г Э. Брандес, В. Мёллер: Параметры безопасности: Том 1: Легковоспламеняющиеся жидкости и газы. Wirtschaftsverlag NW - Verlag für neue Wissenschaft, Бремерхафен, 2003 г.
- ↑ Европейское химическое агентство (ECHA): Заключение по оценке веществ и отчет об оценке .
- ↑ Скользящий план действий Сообщества ( CoRAP ) Европейского химического агентства (ECHA): Метилметакрилат , по состоянию на 26 марта 2019 г.






