Треонин
| Структурная формула | ||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|

| ||||||||||||||||||||||
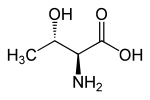
| Структурная формула L- треонина, природного изомера | ||||||||||||||||||||||
| Общий | ||||||||||||||||||||||
| Фамилия | Треонин | |||||||||||||||||||||
| Другие названия |
|
|||||||||||||||||||||
| Молекулярная формула | C 4 H 9 НЕТ 3 | |||||||||||||||||||||
| Краткое описание |
бесцветное твердое вещество с характерным запахом |
|||||||||||||||||||||
| Внешние идентификаторы / базы данных | ||||||||||||||||||||||
| ||||||||||||||||||||||
| Информация о наркотиках | ||||||||||||||||||||||
| Код УВД | ||||||||||||||||||||||
| характеристики | ||||||||||||||||||||||
| Молярная масса | 119,12 г · моль -1 | |||||||||||||||||||||
| Физическое состояние |
твердо |
|||||||||||||||||||||
| Температура плавления |
255 ° C ( разложение , L- треонин) |
|||||||||||||||||||||
| значение pK s |
|
|||||||||||||||||||||
| растворимость |
|
|||||||||||||||||||||
| Инструкции по технике безопасности | ||||||||||||||||||||||
| ||||||||||||||||||||||
| Токсикологические данные | ||||||||||||||||||||||
| Насколько это возможно и общепринято, используются единицы СИ . Если не указано иное, приведенные данные относятся к стандартным условиям . | ||||||||||||||||||||||
Треонин , Thr или Т для короткого , является существенным протеиногенным α - аминокислоты , в его естественном L форме .
В треонине есть гидроксильная группа на β-атоме углерода (= 3-положение) ; он также может рассматриваться как 3-метил - серин или 3-гидроксилированным desmethyl- валина . Из-за гидроксильной группы треонин гораздо более полярен и реакционноспособен, чем валин.
Треонин - одна из полярных аминокислот. Он может фосфорилироваться по своей гидроксильной группе, которая может играть роль в регуляции ферментов.
Стереохимия
Треонин имеет два стереогенных центра на атомах углерода во 2- и 3-положениях. Следовательно, существует четыре стереоизомера треонина со следующими абсолютными конфигурациями: (2 S , 3 R ), (2 R , 3 S ), (2 S , 3 S ) и (2 R , 3 R ). Связанные белки, содержащиеся в L- треонине, имеют (2 S , 3 R ) конфигурацию, а также упомянутые (2 S , 3 R амино-3-гидроксибутановая кислота, -2 (обозначение согласно) IUPAC - Nomenclature ). Остальные три стереоизомера [(2 R , 3 S ) -реонин, (2 S , 3 S ) -аллотреонин и (2 R , 3 R ) -аллотреонин ] L- треонина не имеют большого значения.
Когда о «треонине» говорят без какого-либо дополнительного названия ( префикса ), его обычно называют L- треонином .
| Изомеры треонина | ||||
| Фамилия | L- треонин | D- треонин | L - алло- треонин | D - алло- треонин |
| Другие названия | (2 S , 3 R ) -2-амино-3-гидроксибутановая кислота | (2 R , 3 S ) -2-амино-3-гидроксибутановая кислота | (2 S , 3 S ) - алло -2-амино-3-гидроксибутановая кислота | (2 R , 3 R ) - алло -2-амино-3-гидроксибутановая кислота |
| Структурная формула |  |
 |
 |

|
| Количество CAS | 72-19-5 | 632-20-2 | 28954-12-3 | 24830-94-2 |
| 80-68-2 (не указано) | ||||
| Номер ЕС | 200-774-1 | 211-171-8 | 249-327-2 | 246-488-0 |
| 201-300-6 (не указано) | ||||
| Информационная карта ECHA | 100 000 704 | 100.010.157 | 100 044 829 | 100.042.247 |
| 100.001.183 (неопределенная) | ||||
| PubChem | 6288 | 69435 | 99289 | 90624 |
| 205 (не указано) | ||||
| DrugBank | DB00156 | DB03700 | - | - |
| - (не указано) | ||||
| Номер FL | 17.021 (не указано) | |||
| Викиданные | Q186521 | Q44073885 | Q27103859 | Q27094610 |
| Q60662943 (не указано) | ||||
Вхождение
Треонин входит в состав белков животного и растительного происхождения . Предполагается, что суточная потребность взрослых составляет около 16 мг на кг массы тела. Следующие ниже примеры содержания треонина относятся к 100 г корма; также приводится процентное содержание общего белка.
| Еда | белок | Треонин | доля |
|---|---|---|---|
| Говядина, сырая | 21,26 г | 849 мг | 4,0% |
| Филе куриной грудки, сырое | 23,09 г | 975 мг | 4,2% |
| Лосось, сырой | 20,42 г | 860 мг | 4,2% |
| Куриное яйцо | 12,58 г | 556 мг | 4,4% |
| Молоко коровье 3,7% жирности | 3,28 г | 148 мг | 4,5% |
| Грецкие орехи | 15,23 г | 596 мг | 3,9% |
| Цельнозерновая мука | 13,70 г | 395 мг | 2,9% |
| Кукурузная мука из непросеянной муки | 6,93 г | 261 мг | 3,8% |
| Рис неочищенный | 7,94 г | 291 мг | 3,7% |
| Горох сушеный | 24,55 г | 872 мг | 3,6% |
Все эти продукты содержат химически связанный L- треонин в качестве белкового компонента, только в исключительных случаях L- треонин свободный . У рыб антизамороженные белки состоят почти исключительно из L- треонина и L- аланина .
история
Американский биохимик Уильям Камминг Роуз в течение своей научной карьеры подробно рассматривал важность аминокислот для питания. В экспериментах на крысах в 1930-х годах он обнаружил, что кормление 19 известными до того момента аминокислотами было недостаточным для роста крыс. Затем он систематически искал другую незаменимую аминокислоту; наконец, ему удалось отделить их от фибрина и идентифицировать по их структуре. С помощью этой аминокислоты, известной как треонин, была открыта последняя из канонических протеиногенных аминокислот. Название треонин было выбрано из-за треозной основной структуры этой аминокислоты.
характеристики
Приведенные здесь данные относятся только к L- треонину и D- треонину.
- Остаточное название: Треонил
- Боковая цепь : гидрофильная
- изоэлектрическая точка : 5,64
- Объем Ван дер Ваальса : 93
- Растворимость липидов : log K OW = −0,7
биосинтез
Поскольку L- треонин является одной из незаменимых аминокислот, L- треонин должен поступать с пищей через белки, содержащие L- треонин. У растений и микроорганизмов, биосинтез L - треонина начинается с L - аспартаты , происхождение которых ( оксалоацетат ) поступает из цикла цитрата . Л -аспартата осуществляется через два промежуточных стадий, с помощью соответствующих ферментов (аспартаты - киназа, аспартатсемиальдегиддегидрогеназа, гомосериндегидрогеназа) для L - гомосерин реализован. На следующей стадии первичный спирт фосфорилируется L- гомосерином с помощью гомосеринкиназы. На последнем этапе этот фосфогомосерин превращается гомосеринфосфатмутафосфатазой (PLP) в L- треонин .
Разборка
Для разбивки, включая структурные формулы, см. Раздел Веб-ссылки
Л треонина является либо ацетальдегида и глицина уменьшается, что имеет треонин альдолазы ( ЕС 4.1.2.5 катализируемой). Аминокислота также может быть преобразована в пропионил-КоА .
Производство
L- треонин можно получить из белковых гидролизатов методом экстракции с помощью ионообменников . Однако сегодня L- треонин производится в основном путем ферментации .
использовать
В качестве компонента растворов для инфузии аминокислот [Aminoplasmal ® (D), Aminosteril ® -N-Hepa (D), Primene ® (A)] для парентерального питания L- треонин, наряду с другими аминокислотами, широко используется в организме человека. медицина. «Диета с определенным химическим составом», вводимая перорально, содержащая L- треонин, была разработана для пациентов с нарушением пищеварения . В этой диете аминокислоты являются источником азота; все жизненно важные питательные вещества находятся в строго определенной форме.
Многие виды зерна имеют слишком низкое содержание незаменимых аминокислот. В результате этого недостатка только одной аминокислоты пригодность всех потребляемых аминокислот падает до значения, определяемого незаменимой аминокислотой («ограничивающей аминокислотой»), содержащейся в слишком небольшом количестве. Пищевая ценность зерна затем увеличивается за счет целенаправленного добавления небольших количеств незаменимых аминокислот, в которых их дефицит. За исключением кукурузы, большинство злаков содержат меньше L- треонина, чем требуется домашнему скоту. Добавление L- треонина в комбикорм широко распространено в кормовой промышленности и, таким образом, сохраняет природные ресурсы.
веб ссылки
Индивидуальные доказательства
- ↑ Запись о THREONINE в базе данных CosIng Комиссии ЕС, по состоянию на 28 декабря 2020 г.
- ↑ a b c технический паспорт треонина (PDF) от Merck , по состоянию на 25 декабря 2019 г.
- ↑ a b Технический паспорт L-треонина, 98 +% от AlfaAesar, по состоянию на 25 декабря 2019 г. ( PDF )(Требуется JavaScript) .
- ^ A b c Карл С. Вестлинг, Дональд Т. Уорнер: изоэлектрические точки треонина и некоторых родственных соединений . В: Журнал биологической химии . Лента 144 , нет. 3 , 1942, стр. 687–690 (английский, jbc.org [PDF]).
- ↑ Запись о L-треонине. В: Römpp Online . Георг Тиме Верлаг, доступ 30 мая 2014 г.
- ↑ Лист данных по треонину от Sigma-Aldrich , по состоянию на 17 октября 2016 г. ( PDF ).
- ↑ Д.Х. Бейкер: Толерантность к аминокислотам с разветвленной цепью у экспериментальных животных и людей , в: J. Nutr. , 2005 , 135 (6) , стр. 1585S-1590S; PMID 15930474 .
- ^ База данных по питательным веществам Министерства сельского хозяйства, 21-е издание.
- ^ GC Barrett: Chemistry and Biochemistry of the Amino Acids , Chapman and Hall, London, New York, 1985, p. 11, ISBN 0-412-23410-6 .
- ↑ С. Хансен: Открытие протеиногенных аминокислот с 1805 г. в Париже по 1935 г. в Иллинойсе. ( Памятка от 15 июня 2016 г. в Интернет-архиве ) Берлин 2015.
- ↑ WC Rose, Эксперименты по кормлению смесями высокоочищенных аминокислот: I. Неадекватность диет, содержащих девятнадцать аминокислот , J Biol Chem, Volume 94, p. 155ff (1931)
- ↑ WC Rose, RH McCoy и CE Meyer, Эксперименты по кормлению смесями высокоочищенных аминокислот: VIII. Выделение и идентификация новой незаменимой аминокислоты , J Biol Chem, Volume 112, pp. 283ff. (1935).
- ↑ Бернд Хоппе и Юрген Мартенс: Аминокислоты - Производство и производство , в: Химия в наше время , 1984 , 18 , стр. 73–86; DOI: 10.1002 / ciuz.19840180302 .
- ↑ a b Ёсихару Идзуми, Ичиро Чибата, Тамио Ито: Производство и использование аминокислот , в: Angewandte Chemie (журнал) , 1978, 90 (3), стр. 187-194; DOI: 10.1002 / anie.19780900307 .
