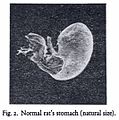
Карцинома Spiroptera
Spiropterakarzinom ([ʃpirɔpterakarʦiˌnoːm] и [SP ...]) находится в желудке инфицированных Spiroptera эксперимента крыс , происходящих увеличение патологической ткани , его открывателем, в датском патологоанатоме Йоханнес Фибигер , по ошибке , как рак был интерпретирован. Казалось, что это доказывает, что рак - заразное заболевание . За это очевидное свидетельство Фибигер получил в 1927 году Нобелевскую премию по физиологии и медицине за 1926 год.
Ошибка не появлялся до 1935 года. С тех пор карцинома Spiroptera считается самой высокой научной ошибкой . Причины этой ошибки заключались в основном в методических ошибках и односторонней интерпретации экспериментальных данных Фибигером. Несмотря на это, карцинома spiroptera оказала большое влияние на экспериментальные исследования рака, которые получили новый импульс и впоследствии привели к выдающимся результатам исследований.
Спустя 70 лет после предполагаемого открытия Фибигером карциномы spiroptera у пациентов с гастритом была обнаружена бактерия Helicobacter pylori , которая является причиной большинства случаев рака желудка во всем мире .
Онкологические знания во времена Фибигера
В начале 20 века инфекционные заболевания, такие как грипп , пневмония , сифилис и туберкулез, были основными причинами смерти населения западного мира. Постепенно выяснилось, какие причины ( этиология ) играют роль в развитии этих заболеваний. Сначала механизмы передачи были выяснены, и бактериальные патогены были идентифицированы с развитием пригодных для использования световых микроскопов . Это позволило разработать первые мощные активные ингредиенты, такие как сальварсан против сифилиса Полом Эрлихом в 1909 году . Напротив, ситуация с раком была совершенно иной. Поиски «возбудителя» не увенчались успехом. Во времена Фибигера существовало три конкурирующих теории о развитии рака, которые активно обсуждались в профессиональных кругах:
- Теория стимулов Рудольфа Вирхова утверждает, что различные внутренние или внешние вредные воздействия ( эндогенные или экзогенные токсины ) приводят к дегенерации клеток: опухоли возникают там, где хронические стимулы действуют на клетки и ткани, но в конечном итоге продолжают расти независимо от эффекта исходного стимула .
- Теория эмбрионального зародышевого рассредоточения по Джулиусу Фридриха Конхейм и Хьюго Рибберта , также известный как теория Cohnheim-Ribbert, предполагает , что рак имеет эмбрионального происхождение и вызывается недифференцированными эмбриональными клетками , которые диспергированные в эмбриональный период . При определенных условиях эти клетки могут привести к неконтролируемому дегенерирующему росту опухоли. Эта теория переживает определенное возрождение в виде раковых стволовых клеток в 21 веке .
- Теория паразитов, с другой стороны, возлагает на паразитов ответственность за развитие рака. Термин «паразит» используется очень широко и также включает другие патогены .
Теория стимулов Вирхова
Ряд свидетельств подтверждают теорию стимулов Вирхова. Например, еще в 1775 году Персивалл Потт с помощью британских трубочистов обнаружил, что рак яичек , который был чрезвычайно распространен в этой профессиональной группе в то время, очевидно , был вызван сажей, которая откладывалась в кожных складках мошонки . В 1895 году Людвиг Рен заметил рост рака мочевого пузыря у химических рабочих, контактировавших с Фуксином . Рак Кангри , который только в Кашмире происходит, был впервые описан в 1881 году. Эта плоскоклеточная карцинома возникает в результате хронического раздражения кожи ( erythema ab igne ), вызванного нагревательной печью, которую носят под одеждой ( кангри ).
С помощью теории стимулов можно объяснить некоторые редкие, довольно экзотические виды рака; Однако он не предоставил каких-либо полезных решений для лечения наиболее распространенных видов рака, например рака груди . Даже Вирхов не исключил наличие «раковой палочки», которую однажды можно обнаружить:
«Доказательства наличия паразитарных микроорганизмов в пораженных частях тела, число которых увеличивалось в течение ряда лет, вселили во многих […] надежду, что раковые палочки также будут обнаружены. Пока результаты даже самых ярых исследований еще не представлены в убедительной демонстрации. Однако возможность такого события нельзя просто игнорировать; да, можно признать, что открытие конкретной бациллы было бы важным шагом вперед в диагностике и прогнозировании карциномы ».
«Вакцинация от рака»
До Фибигера была некоторая новаторская работа по экспериментальному образованию рака у модельных организмов. Российский ветеринар Мстислав Александрович Новинский (1841-1914) пересаживал злокачественные опухоли собак щенкам между 1875 и 1876 годами , которые росли там, частично метастазировали и, в свою очередь, могли быть трансплантированы другим щенкам. В 1889 году немецкому патологу Артуру Натану Ханау (1858–1900) удалось трансплантировать эпидермальную карциному вульвы от крыс к другим крысам, т.е. осуществить перенос гомологичной опухоли («вакцинация от рака»). Однако результаты этих тестов показали только возможность передачи существующего заболевания другому человеку. Однако они не помогли выяснить причины рака.
Впервые искусственное создание раковой опухоли у экспериментального животного было осуществлено в 1915 году - через два года после публикации работы Фибигера - японцем Кацусабуро Ямагива (1863–1930) и его помощником Коичи Итикава . Они чистили внутренности ушей морских свинок дегтярным маслом . Примерно через 250 дней на обработанных таким образом участках кожи образовались опухоли. С сегодняшней точки зрения, работа Ямагивы была новаторской и положила начало совершенно новой области работы в экспериментальной онкологии .
Теория паразитов
У теории паразитов было много последователей во времена Фибигера. Еще в 1911 году районный врач Кенигсберга Ганс Абрамовский утверждал, что червь Opisthorchis febriens является канцерогеном, который передается человеку при употреблении в пищу сырой или недоваренной рыбы. Червь, который предпочитает колонизировать желчные протоки и поджелудочную железу, может вызвать рак из- за хронического воспаления этих органов.
Leiden профессор Reinder Питер ван калькара увидел причину рака в простейших , которые , в свою очередь , колонизировали нематода. Он сам привил собакам простейшие, которых выделил от кишечных паразитов и тараканов. Затем он обнаружил инфильтративно растущие и метастазирующие «злокачественные аденомы » и карциномы у подопытных животных . Результаты чистки дегтем, которые на самом деле являются четким указанием на теорию стимулов Вирхова, были приписаны действию простейших. Ван Калькар обнаружил в своих экспериментах, что у животных, которых он защищал от контакта с простейшими с помощью специальных защитных мер, развивались карциномы реже, чем в группе сравнения.
Генетическая модификация из-за онкогенов
Генрих Вильгельм Вальдейер заложил основы современного состояния знаний о раке еще в 1867 году. Он предположил, что рак возникает в результате индуцированного преобразования нормальных клеток в злокачественные. Эти вырожденные клетки сначала размножаются локально, проникают в здоровые ткани (инфильтрация), а затем распространяются по лимфатической или кровеносной системе (метастазы). Однако замечания Вальдейера носили чисто описательный характер и, следовательно, не содержали никаких заявлений о механизмах развития рака. В 1914 году, через год после первой публикации Фибигера о карциноме spiroptera, Теодор Бовери представил новаторские подходы к этому со своими постулатами, которые действуют и сегодня. Бовери предположил, что рак развивается из одной клетки, генетическая информация которой ранее была изменена. Он подозревал, что генетическая информация находится в хромосомах . Он видел опухоли как результат аномальной хромосомной конституции. В отношении развития опухоли он подозревал эволюцию опухолевых клеток в сторону увеличения злокачественности. Клетки потеряют определенные свойства, особенно способность реагировать на сигналы от других клеток. Это приводит к автономии опухолевых клеток. Он также подозревал, что в нормальных клетках есть гены, подавляющие рост клеток. Потеря этих генов приведет к трансформации в раковые клетки. Бовери умер через год после публикации, и его постулаты были давно забыты.
Первый онкоген был открыт Фрэнсисом Пейтоном Роусом в 1911 году. Используя бесклеточный ультрафильтрованный экстракт мышечной опухоли ( саркомы ) курицы , он смог вызвать новые опухоли у других цыплят, вводя его другим цыплятам. Бактерия или даже многоклеточный паразит могут быть исключены как патоген, поскольку они полностью отделены фильтром. Раус подозревал, что в этом экстракте есть вирус. О вирусах, которые в то время нельзя было сделать видимыми, было известно очень мало. Позднее вирус был обнаружен и назван вирусом саркомы Рауса в честь Рауса . Сегодня онкоген вируса саркомы Рауса считается доказательством того, что измененные гены могут быть причиной рака.
Открытие Фибигера
С 1900 Johannes Фибигер был профессор и директор Института патологической анатомии в в Копенгагенском университете . В 1907 году во время гистологических исследований желудков диких коричневых крыс ( Rattus norvegicus ) и домашних крыс ( Rattus rattus ) он заметил, что многие туши животных в лесном желудке имели эпителиальную гиперплазию с образованием папиллом . Однако эти опухоли не дали метастазов и не проникли в окружающую здоровую ткань . Эти опухоли не колонизировали другие области пищеварительного тракта . Однако, к своему удивлению, он обнаружил аскариды (нематоды) и их яйца в некоторых из этих опухолей . Нематода была идентифицирована Хьялмаром Дитлевсеном , ассистентом Зоологического музея Копенгагенского университета, как новый вид нематод, принадлежащий к «группе спироптерид». В нижеследующем подробном зоологическом описании нематода получила видовое название Spiroptera neoplastica . Эпитет neoplastica выбрал Фибигер и Ditlevsen из - за предполагаемый эффект нематоды, неоплазия «(от древнего греческого νέος ОСЗА » новой»и πλάσσειν plassein , форма„формы“, новогреческий : δυσπλασία ), так новообразований = опухоль. 1915 представил американский зоолог Брайтона Говард Ransom обнаружил , что Spiroptera neoplastica определенно вид из Gongylonema принадлежит. Поэтому он предположил, что в будущем этот недавно обнаруженный вид должен называться Gongylonema neoplasticum . Дитлевсен согласился с предложением Рэнсома, и с тех пор этот вид нематод, для которого нет названия на немецком языке, получил название Gongylonema neoplasticum . На момент открытия Фибигера уже были сообщения о «раковых бациллах» и различных паразитах, которые были связаны с развитием рака, но ни одному исследователю не удалось экспериментально искусственно и преднамеренно вызвать раковые опухоли у подопытных животных . Возможность сделать это первым была движущей силой дальнейшей работы Fibiger.
После своего первого вскрытия Фибигер исследовал более 1000 желудков мышей и крыс, но не обнаружил «карциномы spiroptera» ни в одном из образцов. Фибигер хотел прекратить работать в этой области, когда он обнаружил опухоли и нематод, которые искал, у крыс с Копенгагенского сахарного завода . Он заметил на фабрике большое количество тараканов , что заставило его поверить в то, что тараканы являются промежуточными хозяевами для Gongylonema neoplasticum . В лабораторных исследованиях Фибигер фактически идентифицировал американского таракана ( Periplaneta americana ) и обыкновенного таракана ( Blatta orientalis ) как промежуточных хозяев для Gongylonema neoplasticum . Он преуспел в передаче Gongylonema neoplasticum на немецкий таракан ( Blattella Germanica ) в качестве промежуточного хозяина.
Нематода первоначально пришла из Южной Америки и Вест-Индии и была доставлена на корабле вместе со своим промежуточным хозяином и сахаром. В своих первых попытках искусственно вызвать раковые опухоли с помощью Gongylonema neoplasticum , Фибигер накормил семь лабораторных крыс американскими тараканами. После естественной смерти подопытных животных он тщательно их обследовал. Во всех из них он обнаружил нематод в лесном животе. У одной крысы он также увидел гиперплазию эпителия, а у двух самых долгоживущих крыс также сильную пролиферацию , глубокий рост и гетеротопию эпителия в сочетании с воспалением и выраженным образованием папиллом. Он интерпретировал это как начало и менее распространенное образование карциномы . Он также смог передать нематоду лабораторным мышам, морским свинкам , лесным мышам , кроликам, белкам ( Sciurus vulgaris ) и коричневогрудым ежам, но не обнаружил образования карциномы ни у одного из этих видов. В более крупной серии экспериментов он накормил 91 «цветную и белую» крысу тараканами. Ранее он кормил тараканов фекалиями крыс, содержащими яйца спироптерых и сахарную воду, так что они проглотили Spiroptera neoplastica в качестве промежуточного хозяина . Крыс обследовали после естественной смерти. Фибигер обнаружил папилломатозные изменения в животе у 22 животных и карциноматные изменения у 12 из этих животных. Он определил инкубационный период от трех до четырех месяцев. У двух животных он обнаружил небольшие метастазы в легких , в которых не было ни нематод, ни их яиц. Фибигер полагал, что опухоли были вызваны токсином нематод.
В 1913 году он впервые опубликовал свои результаты. Во введении к этой статье он сослался на результаты Стефаноса Картулиса , который часто диагностировал рак мочевого пузыря, вызванный сосальщиками Schistosoma haematobium , у пациентов с шистосомозом (шистосомозом) . Публикация Фибигера произвела фурор в профессиональном мире, потому что он, казалось, был первым, кому удалось экспериментально запустить злокачественную опухоль. Казалось, открываются совершенно новые возможности для исследования патогенеза рака и будущих методов лечения. Вскоре после публикации «Фибигер» получил множество различных наград. Например, он стал членом престижного Шведского медицинского общества ( Svenska Läkaresällskapet ). Датское медицинское общество избрало его своим президентом Комиссии по раку. Затем последовали многочисленные почетные докторские степени различных известных университетов. Позднее Фибигер сообщил об успешной подкожной трансплантации карциномы spiroptera, например, в течение четырех поколений мышам.
- Представления с лекции Фибигера о вручении Нобелевской премии 12 декабря 1927 г.
Номинации на Нобелевскую премию Фибигера
Между 1922 и 1927 годами Иоганнес Фибигер был номинирован различными учеными на Нобелевскую премию по физиологии и медицине в общей сложности шестнадцать раз . Поэтому его работа несколько раз подвергалась особой проверке Нобелевским комитетом по физиологии и медицине . В 1922 и 1923 годах член комитета Гуннар Хедрен постановил, что Фибигер не принес «величайшую пользу человечеству» своим открытием , как Альфред Нобель хотел сделать для получения премии в области физиологии и медицины. Он рекомендовал дождаться окончательного суждения о достоинствах открытия Фибигера, прежде чем присуждать награду.
В 1926 году Фибигер получил три номинации. Его работа была снова рассмотрена вместе с работой Кацусабуро Ямагивы, который также был номинирован. Также Феликс Юбер д'Эрелль и Отто Варбург были номинированы на Нобелевскую премию 1926 года. Нобелевский комитет запросил два отдельных отчета о работе Фибигера и Ямагивы. Два шведских патологоанатома Фольке Хеншен и Хильдинг Бергстранд , оба профессора Каролинского института , подготовили отчет по каждому кандидату. Хеншен высоко оценил работу Фибигера и ее значительное влияние на исследования рака в целом. Он процитировал известного исследователя рака Арчибальда Лейтча :
«Но новая эра исследований рака началась, когда Йоханнес Фибигер из Копенгагена представил свои блестящие эксперименты по развитию рака желудка у крыс. Тогда впервые можно было сказать, что рак, вне всяких сомнений, возник экспериментальным путем, и исследование этиологии рака превратилось в практическую задачу ».
«Новая эра в исследованиях рака началась, когда Йоханнес Фибигер из Копенгагена представил свои блестящие эксперименты по индуцированию рака желудка у крыс. В результате, рак впервые, без всяких сомнений, мог быть вызван экспериментально, а исследование его этиологии стало практической задачей ».
Хеншен, который был личным другом Фибигера, также очень положительно отозвался об открытии Ямагивы. Ямагива был вдохновлен работой Фибигера, опубликованной за два года до него. В отличие от Fibiger, очистка дегтя Yamagiwa зарекомендовала себя как метод экспериментального производства рака в онкологии. Это было намного проще выполнить, и результаты были воспроизводимы. Щетка для дегтя использовалась в онкологических лабораториях по всему миру и уже сделала возможными некоторые новые открытия и разработки. Хеншен пришел к выводу, что экспериментальные карциномы достойны Нобелевской премии, и предложил разделить цену между Фибигером (за открытие экспериментальной карциномы паукообразных) и Ямагивой (за открытие экспериментальной карциномы дегтя).
Бергстранд же пришел к гораздо более сдержанному результату. Хотя он отдавал должное работе Фибигера и Ямагивы, он видел в них лишь экспериментальное подтверждение давно известных клинических фактов. В качестве примера он привел связанные с работой раковые заболевания у трубочистов и радиологов. Кроме того, ни одно из открытий не внесло никакого вклада в выяснение происхождения злокачественных опухолей. Буквально он утверждал:
«Экспериментальное подтверждение ранее известного факта, конечно, всегда приветствуется, хотя его важность в данном случае не может считаться значимостью того, что оно достойно Нобелевской премии».
«Экспериментальное подтверждение ранее известного факта, конечно, всегда хорошо, но в этом случае значение не может считаться достаточным, чтобы быть достойным Нобелевской премии».
Бергстранд также поставил под сомнение будущее значение обоих открытий для исследования рака. Он считал, что результаты других исследователей, а именно Отто Варбурга, станут более важными в будущем. В своем резюме он сомневался, что результаты двух номинантов будут иметь какое-либо большое значение для решения загадки рака. Оба открытия не достойны Нобелевской премии.
В результате между Хеншеном и Бергстрандом возник спор . Это произошло, когда Бергстранд настоятельно рекомендовал Феликсу Юберу д'Эреллю получить награду. Хеншен отклонил д'Эрелля как лауреата, потому что он работал не один в этой области, и он один не мог удостоиться чести открывать бактериофаги. Комитет запросил третье мнение у Джона Сьёквиста . Подтвержденная оценка Хеншеном работы д'Эреля. Отказ Бергстранда в конечном итоге привел к тому, что Хеншен отказался от своего предложения о совместной Нобелевской премии и теперь выступал за вручение премии только Фибигеру. В конце концов Нобелевский комитет решил не присуждать Нобелевскую премию 1926 года по физиологии и медицине .
В 1927 году Каролинский институт получил семь номинаций на Fibiger. Был заказан еще один специальный обзор. Также были номинированы Отто Варбург, Юлиус Вагнер-Яурегг и Чарльз Скотт Шеррингтон . Комитет снова поручил Хеншену и Бергстранду подготовить отчет; на этот раз о Фибигере и Варбурге, по одному отчету на каждого рецензента. В этом году мнения двух экспертов по Fibiger также сильно разошлись. Бергстранд признал импульс и вдохновение работы Фибигера по исследованию рака, но в конечном итоге это было просто доказательством вековой теории. Он также признал, что Ямагива был вдохновлен работой Фибигера, но что его работа является полностью независимым достижением. Он снова поставил под сомнение клиническую значимость открытия Фибигера, которое до сих пор не внесло никакого вклада в выяснение этиологии спонтанных опухолей у людей. В своем отчете Хеншен пришел к совершенно иному выводу. Прошедший год еще больше укрепил его мнение об открытии Фибигера. Количество писем о номинациях, полученных комитетом от высокопоставленных ученых в этом году, также подтверждает его мнение. Он подчеркнул, что Фибигер дал толчок всем исследованиям рака, о которых также упоминал Бергстранд, особенно в то время, когда в онкологии не было прогресса. С Fibiger началась новая эра в исследованиях рака. Однако в случае с Отто Варбургом Бергстранд и Хеншен пришли к такому же выводу. Варбург был номинирован за свою гипотезу о том, что раковые клетки обладают особым анаэробным метаболизмом. Оба эксперта подвергли критике тот факт, что фактов, на которых основывалась гипотеза Варбурга, было недостаточно. Работу Варбурга оценил третий рецензент, Эйнар Хаммарстен , профессор химии и фармации Каролинского института. В отличие от Бергстранда и Хеншена, Хаммарстен был убежден в важности открытия Варбурга. На основе этих трех отчетов комитет пришел к выводу, что и Варбург, и Фибигер достойны Нобелевской премии. Он единогласно предложил, чтобы половина Нобелевской премии по физиологии и медицине, которая не была присуждена в прошлом году, была присуждена Варбургу и Фибигеру, а награда 1927 года - Юлиусу Вагнер-Яуреггу «за открытие терапевтического значения вакцинации против малярии в лечение прогрессирующего паралича ».
Однако Нобелевская ассамблея Каролинского института отклонила предложение комитета и распорядилась, чтобы Фибигер получил премию только за 1926 год. Причины этого решения пока неизвестны. Отто Варбург получил Нобелевскую премию по физиологии и медицине в 1931 году.
В 1927 г. удостоен Нобелевской премии Фибигеру.
Йоханнес Фибигер получил Нобелевскую премию за то, что первым сумел воспроизвести рак у лабораторных животных в контролируемом эксперименте. Восхваление на 10 декабря 1927 года был дан Вильгельм Вернштедт (1872-1969), декан Каролинского института. Вернштедт сказал, что долгое время считалось, что существует причинная связь между раком и длительным механическим, термическим, химическим или актиническим раздражением тканей. В некоторых случаях это профессиональные заболевания. Например, рак у радиологов, трубочистов и химиков являются примерами раковых инфекций, которые, по мнению некоторых, вызваны радиоактивностью или химическим раздражением. Однако все попытки вызвать этот рак у лабораторных животных потерпели неудачу. Поиск «раковой палочки» как причины рака также не увенчался успехом. Черви также считались возможными причинами рака, но сторонники этой теории часто рассматривались как мечтатели . В то время, когда не было четкого представления о причине рака, Фибигер был первым, кому удалось экспериментально вызвать рак в 1913 году. Впервые экспериментальное превращение нормальных клеток в раковые было успешным. Было убедительно показано, что рак не всегда вызывается червем, но рак может быть вызван внешним раздражителем. Уже по этой причине открытие Фибигера имеет неоценимое значение. В своих дальнейших замечаниях Вернштедт подчеркнул, что работы Фибигера дали импульс исследованиям рака в целом. За эту бессмертную исследовательскую работу Йоханнес Фибигер был бы удостоен Нобелевской премии по медицине в 1926 году в тот же день (« Именно за эту бессмертную исследовательскую работу Фибигер получил сегодня Нобелевскую премию по медицине 1926 года »).
Два дня спустя Фибигер прочитал свою лекцию на английском языке в Каролинском институте, получившую Нобелевскую премию. Во-первых, он размышлял о работе Артура Натана Ханау и Анри Моро по трансплантации опухолей, а также о трех важных теориях развития рака того времени: теории стимулов Вирхова, теории распространения зародышевых зародышей Конхейма и теории, согласно которой рак приписывают паразитам. До недавнего времени все попытки вызвать рак у здоровых подопытных животных с помощью химических или физических стимулов или путем трансплантации эмбриональной ткани и различных микроорганизмов были безуспешными. Он кратко упомянул результаты французской рабочей группы, которая преуспела в 1910 году в создании раковых опухолей с помощью рентгеновских лучей, а также эксперименты Пейтона Рауса с «невидимыми вирусами». Однако он упомянул о сохраняющихся сомнениях относительно того, действительно ли образование новой ткани было «настоящим раком». С нематодой Gongylonema neoplasticum был разработан первый успешный метод систематического экспериментального получения рака у лабораторных животных. Далее Фибигер подробно рассказал о своих исследованиях карциномы spiroptera. Затем он заболел раком человека, вызванным червями, такими как пара пиявок. Gongylonema neoplasticum никогда не был обнаружен у человека, кроме родственного ему червя Gongylonema pulchrum . Однако ни одного случая рака, вызванного G. pulchrum, не известно. Вообще, пока нет доказательств того, что черви играют важную этиологическую роль в патологии рака у человека. Из результатов его исследований также нельзя сделать вывод, что рак обычно вызывается паразитами. Он интерпретировал результаты своей работы по карциноме spiroptera как доказательство теории стимулов Вирхова. Он подозревал, что канцерогенное действие некоторых червей было вызвано выделением нематодами канцерогенных токсинов. В дальнейшем в своей лекции Фибигер остановился на предрасположенности к раку. Возраст - главный фактор предрасположенности к раку. Это давно принятая доктрина для всех типов рака. Результаты его экспериментов с карциномой spiroptera, а также другие попытки вызвать рак у лабораторных животных, например, путем нанесения смолы, противоречат этой доктрине. В тех же условиях испытаний у молодых подопытных животных опухоли развивались бы так же часто и так же быстро, как и у старых подопытных животных. В конце своей лекции он повторил заявление о том, что до сих пор нет убедительных доказательств микробного происхождения рака у людей, даже если более поздние исследования показывают, что микропаразиты и вирусы могут вызывать рак.
Всего через несколько недель после получения Нобелевской премии Иоганнес Фибигер умер 30 января 1928 года в Копенгагене. Он скончался от сердечной недостаточности после того, как множественные флеботромбозы привели к массивной тромбоэмболии легочной артерии . Он также страдал колоректальным раком, поэтому ему сделали коэкостомию .
Опровержение результатов Фибигера
В 1918 году, через пять лет после первой публикации об искусственном поколении карциномы spiroptera, гистологические открытия Фибигера были подвергнуты сомнению Фредериком Д. Баллоком и Джорджем Л. Роденбургом из Колумбийского университета . Они пришли к выводу, что клеточные изменения - это не карциномы, а гипертрофия эпителия слизистой оболочки желудка . Однако репутация Fibiger быстро положила конец критике. Кроме того, другие известные гистопатологи также пришли к выводу, что это были карциномы. Следует отметить, что в то время гистологические методы все еще находились в зачаточном состоянии и никоим образом не были стандартизированы . В последующие годы ни одному другому исследователю рака не удалось воспроизвести результаты Фибигера. Опухоли у подопытных животных обнаруживались очень редко. Причины этого до сих пор окончательно не выяснены, но есть ряд указаний. Однако можно сказать наверняка, что «раковые опухоли», описанные Фибигером, не были злокачественными изменениями и что нематоды, обнаруженные в опухолях, не были ответственны за наблюдаемый доброкачественный рост клеток.
Чтобы опровергнуть выводы Фибигера, потребуется более 20 лет. Одна из причин этого заключается в том, что метод Фибигера редко использовался исследователями рака из-за его сложности. Очистка дегтем от Ямагива, которую намного проще выполнять, дала значительно более воспроизводимые результаты и была гораздо более популярной среди экспертов. В 1935 году рабочая группа под руководством онколога Ричарда Дугласа Пасси (1888–1971) из Университета Лидса опубликовала результаты своего исследования карциномы spiroptera. Пасси и его коллеги обнаружили, что у инфицированных подопытных животных не развивались раковые опухоли, если им давали полноценную диету. В метастазах в легких в Fibigers экспериментах - так Passeys гипотезы - отсутствие витамина А срабатывает. У людей также известно, что гиповитаминоз витамина А способствует образованию раковых опухолей, особенно в эпителии слизистых оболочек. Пасси подозревал, что гиповитаминоз в экспериментах Фибигера на животных усилил инфекцию, вызванную нематодами, и что раздражение слизистой оболочки желудка, возможно, привело к предполагаемым наблюдаемым карциномам. Гистологические записи доброкачественных изменений, опубликованные рабочей группой, очень похожи на фотографии Фибигера.
В 1952 году два американца Клод Р. Хичкок и Элексиус Т. Белл повторили эксперименты Фибигера в Университете Миннесоты . Однако они изменили его так, что некоторые из подопытных животных получали достаточное количество витамина А, в то время как другая часть получала этот витамин в недостаточном количестве. Фибигер кормил своих подопытных животных белым хлебом и водой. Из разговоров с несколькими пекарями Хичкок и Белл выяснили, что существует очень высокая вероятность того, что белый хлеб Фибигера не содержит ни яиц, ни молока , то есть в основном не содержит витамина А. У своих подопытных животных с дефицитом витамина А они обнаружили, помимо нематодной инфекции, далеко идущие «раковые» папилломы, описанные Фибигером. Они определили эти изменения как доброкачественные. Когда они изучили микрофотографии Фибигера, они пришли к выводу, что это тоже были доброкачественные изменения.
Ошибка фибигера
В то время, когда Фибигер проводил свои эксперименты, в исследованиях рака редко проводились контролируемые исследования . С группой сравнения животных, которые содержались в идентичных условиях и кормили неинфицированных тараканов вместо инфицированных тараканов (« группа плацебо »), была бы высокая вероятность того, что результаты теста не были бы неправильно истолкованы. Парадоксально, но сам Фибигер был одним из первых ученых, которые провели рандомизированные контролируемые испытания, например, в своих исследованиях дифтерии, но не в исследованиях карциномы паукообразных. Его подопытные животные были в основном дикими крысами, которые, в зависимости от их возраста, предыдущего образа жизни и происхождения, вносили значительные неконтролируемые колебания в каждую серию испытаний. Сегодня для научных экспериментов используются специально выведенные животные, которые имеют минимально возможные различия и одного возраста. Во времена Фибигера потребность в сбалансированной диете для лабораторных животных была неизвестна, так же как недостаток витамина А способствовал развитию спонтанных опухолей.
Прием и последствия
Плохая воспроизводимость экспериментальной индукции рака и ошибки при присуждении Нобелевской премии Фибигеру вызвали значительную неуверенность в ответственном Нобелевском комитете в последующие годы. Пройдет 40 лет, прежде чем онколог снова получит эту премию. Очень старый Фрэнсис Пейтон Роус получил его в 1966 году для «своих открытий в области онкогенных вирусов», которые он сделал в 1910 году.
В 1950-х годах пищеводный червь ( Spirocerca lupi ) был идентифицирован как паразит, аналогичный Gongylonema neoplasticum , который, как было показано, вызывает рак пищевода у собак .
Ровно через 70 лет после предполагаемого открытия Фибигером карциномы spiroptera два австралийских доктора Барри Маршалл и Джон Робин Уоррен обнаружили бактерию Helicobacter pylori в биопсиях желудка у пациентов с гастритом в 1983 году . Они обнаружили, что эта бактерия ответственна за ряд желудочных заболеваний, в частности, за рак желудка. Рак желудка является второй по значимости причиной смерти от рака после рака легких: ежегодно во всем мире умирает более 700 000 человек. Маршалл и Уоррен получили Нобелевскую премию по физиологии и медицине 2005 года за свою работу над H. pylori .
Сегодняшняя научно принятая модель развития рака основана на работах Теодора Бовери и Карла Генриха Бауэра . Согласно этим результатам, рак - это генетическое заболевание. Переход от клеток организма к опухолевым происходит через генетические изменения. Внешние факторы, такие как определенные стимулы, например ионизирующее излучение, определенные химические вещества, вирусы, бактерии или хронические воспалительные процессы, могут способствовать или, по крайней мере, ускорять переход. Теория мутации Бауэра могла быть подтверждена экспериментально с помощью анализа ДНК в конце 20-го века. Таким образом, теория паразитов сегодня устарела , даже если некоторые паразиты могут вызывать злокачественные опухоли через хроническое раздражение. Распознаваемая причинная цепь в этом случае: паразит → хронический стимул = хроническое воспаление → модификация гена → опухоль, а не паразит → опухоль . Несмотря на эти результаты, в определенных кругах альтернативной медицины все еще отстаиваются другие тезисы о развитии рака. Например, российский химик Тамара Лебедева с середины 1990-х распространяет утверждение, что все виды рака вызываются одноклеточной Trichomonas vaginalis . Так называемая терапия Кларка также основана на теории, что рак неизменно вызывается паразитами, особенно пиявками, такими как гигантские кишечные пиявки .
литература
- Анита Кильдебаек Нильсен, Эйвинд Б. Торлинг: Йоханнес Фибигер (физиология или медицина, 1926 г.) - Ставить не на ту лошадь? В: Генри Нильсен, Келд Нильсен (ред.): Нобелевский сосед: История тринадцати датских Нобелевских премий. Глава 14, Издательство Орхусского университета, 2001, стр. 461f. ISBN 87-7288-899-7 .
- IM Modlin, M. Kidd, T. Hinoue: О Фибигере и баснях: поучительная история о тараканах и Helicobacter pylori. В кн . : Журнал клинической гастроэнтерологии. Том 33, номер 3, сентябрь 2001 г., стр. 177-179, ISSN 0192-0790 . PMID 11500602 .
- Й. Клеммезен: Йоханнес Фибигер. Гонгилонема и витамин А в канцерогенезе. В: Acta patologica et microbiologica Scandinavica. Добавка. Номер 270, 1978, стр. 1-13, PMID 362817 .
- Йоран Лильестранд: Премия в области физиологии и медицины. В: Нобелевский фонд (Ред.): Нобель, человек и его премии. 3-е издание, Elsevier, 2007, ISBN 1-4067-4114-0 , стр. 139-277.
- JC Petithory, J. Théodoridès, L. Brumpt: оспариваемая Нобелевская премия: Johannes Fibiger, 1926. В: Histoire des Sciences médicales. Volume 31, Number 1, 1997, pp. 87-95, ISSN 0440-8888 . PMID 11625107 . (Французский)
Сноски
- ↑ Описано Fibiger Mus decumanus , как это было принято в то время.
- ↑ Описано Fibiger Mus rattus , как это было принято в то время.
- ↑ Из Фибигера, как упоминается Periplaneta orientalis
- ↑ Из Фибигера, как упоминается Phyllodromia germanica.
Индивидуальные доказательства
- ↑ К. Кирхгоф: Гений и ошибка. (PDF; 161 kB) В: MaxPlanckResearch , Heft 3, 2008 г., стр. 58–59.
- ↑ Ю. Горина и др.: Тенденции причин смерти среди пожилых людей в США. (PDF; 359 kB) В: Тенденции старения . № 6, Национальный центр статистики здравоохранения, 2006 г., на основе данных из журнала «Смерти: основные причины 2002 г.» NVSR, Vol. 53, No. 17.
- ↑ Р. Вирхов: Патологические опухоли. 30 лекций, проведенных в течение зимнего семестра 1862–1863 гг. В Берлинском университете. Том 1, Август Хиршвальд 1863 г., стр.74.
- ^ Дж. Конхейм: Лекции по общей патологии. Справочник для врачей и студентов. 2-е издание, том 1.2, Берлин, 1882 г.
- ^ Sell: Происхождение стволовых клеток рака и дифференцировочная терапия. В: Критические обзоры в онкологической гематологии . Volume 51, Number 1, July 2004, pp. 1-28, ISSN 1040-8428 . DOI: 10.1016 / j.critrevonc.2004.04.007 . PMID 15207251 . (Рассмотрение).
- ↑ Р. Бехла: О повышенной и эндемической заболеваемости раком. В: Zentralblatt für Bakteriologie . Том 24, с. 875-879. ограниченный предварительный просмотр в поиске книг Google
- ↑ а б Х. Абрамовский: К теории паразитарного рака. В: Журнал исследований рака . Том 9, номер 2, 1910, стр. 385-391. ISSN 1432-1335
- ↑ Макс Моссе, Густав Тугендрайх: Болезни и социальная ситуация. JF Lehmanns, 1913, стр. 609.
- ↑ Вольфганг Хиддеманн , Клаус Р. Бартрам : Die Onkologie. 2-е издание, Springer, 2009 г., ISBN 3-540-79725-4 , стр. 199. Ограниченный предварительный просмотр в поиске книг Google
- ↑ EF Neve: Кангри-ожоговый рак. В: Британский медицинский журнал. Том 2, номер 3287, декабрь 1923 г., стр. 1255-1256, ISSN 0007-1447 . PMID 20771404 . PMC 2317796 (полный текст).
- ↑ SV Gothoskar, KJ Ranadive: Экспериментальные исследования этиологии «рака Кангри». В: Британский журнал рака . Том 20, номер 4, декабрь 1966 г., стр. 751-755, ISSN 0007-0920 . PMID 5964606 . PMC 2008146 (свободный полный текст).
- ↑ Ханс-Вернер Альтманн, Франц Бюхнер: Справочник по общей патологии. Том 6, Springer, 1956, с. 376.
- ↑ Р. Вирхов: О диагностике и прогнозе рака. В: Архивы патологической анатомии и физиологии и клинической медицины . Том 111, выпуск 1, 1888 г., стр. 1-24.
- ↑ a b c К. Людтке: О разрешимости научных споров - обсуждается на примере спора в более ранних исследованиях опухолей. (PDF; 536 kB) В: Препринт. Том 214, Институт истории науки Макса Планка, 2002 г.
- ^ Р. Нери: Рак: загадка в биологии и обществе. Тейлор и Фрэнсис, 1986, ISBN 0-7099-1825-9 , стр. 126. Ограниченный предварительный просмотр в Поиске книг Google
- ^ HW Bucher: О первой гомологичной передаче опухоли в Цюрихе Артуром Ханау в 1889 году. В: Gesnerus . Том 21, 1964, стр. 193-200, ISSN 0016-9161 . PMID 14279710 .
- ↑ М.Б. Шимкин: Артур Натан Ханау: дальнейшая заметка по истории трансплантации опухолей. В кн . : Рак . Том 13, 1960, с. 221, ISSN 0008-543X . PMID 14446015 .
- ↑ К. Ямагива, К. Итикава: Экспериментальное исследование патогенеза эпителиальных опухолей. В: Коммуникационный медицинский факультет Univ Tokyo. Том 15, номер 2, 1915 г., стр. 295-344.
- ↑ К. Ямагива, К. Итикава: Об искусственном производстве папилломы. В: Verh Jpn Path Ges. Том 5, 1915, стр. 142-148.
- ↑ Кацусабуро Ямагива (1863-1930). В: CA. Том 27, номер 3, 1977 г., стр. 172-173, ISSN 0007-9235 . PMID 406017 .
- ^ Ф. Хеншен : рак дегтя Ямагива и его историческое значение. От Персиваля Потта до Кацусабуро Ямагивы. В: Ганн. Том 59, номер 6, декабрь 1968 г., стр. 447-451, ISSN 0016-450X . PMID 4889459 .
- ↑ Х. Абрамовски: Предрасположенность и раздражение при раке. В: Журнал исследований рака. Том 10, номер 2, 1911 г., стр. 235-246.
- ^ RP van Calcar: Причина рака. ван Дусбург, 1926 год.
- ↑ Вальдейер: Развитие карцином. В: Арка Вирхова. Том 41, 1867 г., стр. 470-523. Полный текст в Поиске книг Google
- ↑ Вальдейер: Развитие карцином. В: Арка Вирхова. Том 55, 1872 г., стр. 67-159.
- ↑ a b Мел Ф. Гривз: Рак - безбилетный пассажир эволюции. Springer, 2002, ISBN 3-540-43669-3 , стр. 34. Ограниченный предварительный просмотр в поиске книг Google.
- ↑ Т. Бовери: К вопросу о развитии злокачественных опухолей, Г. Фишер, 1914.
- ↑ а б в Герхард Готтшалк : Ген и человек. Академия наук, Wallstein Verlag, 2000, ISBN 3-89244-405-6 , стр. 192. Ограниченный предварительный просмотр в поиске книг Google
- ↑ Ульрих Вольф: Теодор Бовери и его книга «К проблеме происхождения злокачественных опухолей». В: Джеймс Герман (ред.): Хромосомы и рак. Wiley & Sons, ISBN 0-471-29682-1 , стр. 3-20.
- ↑ б с д е е г ч я J J. Фибигера: Исследования по Spiroptera карциномы и экспериментальной индукции рака. Нобелевская лекция, 12 декабря 1927 г.
- ↑ a b c d e f g h i j k l m CM Stolt, G. Klein, AT Jansson: Анализ ошибочной Нобелевской премии имени Йоханнеса Фибигера, 1926: исследование в Нобелевских архивах. (PDF; 97 kB) В: Достижения в исследованиях рака . Том 92, 2004, стр. 1-12, ISSN 0065-230X . DOI: 10.1016 / S0065-230X (04) 92001-5 . PMID 15530554 .
- ↑ а б в Дж. Фибигер: Дальнейшие исследования спироптеракарциномы крысы. В: Журнал исследований рака. Том 14, номер 2, 1914 г., стр. 295-326.
- ↑ Дж. Фибигер: Исследования карциномы Spiroptera крысы и мыши. В: Журнал исследований рака. Том 16, номер 1, 1920 г., стр. 1-79.
- ↑ б с д е Генрих Zankl : Нобелевские премии. John Wiley & Sons, 2012, ISBN 3-527-64146-7 , стр. 101-104. ограниченный предварительный просмотр в поиске книг Google
- ↑ а б Дж. Фибигер: Исследования нематоды (Spiroptera sp. N.) и ее способности вызывать папилломатозные и карциноматозные опухолевые образования в желудке крысы. В: Журнал исследований рака. Том 13, номер 2, 1913 г., стр. 217-280.
- ^ С. Картулис: Дальнейшие вклады в патологическую анатомию Bilharzia (Distomum haematobium, Cobbold). В: Архив Вирхова . Том 152, номер 3, стр. 474-486. ISSN 1432-2307
- ^ Фрэнк Нортен Мэджилл: Лауреаты Нобелевской премии: 1901-1944. , Салем Пресс, 1991, ISBN 0-89356-572-5 , стр. 267.
- ↑ Речь на церемонии награждения. Похвала Вернштедта, произнесенная 10 декабря 1927 года в Стокгольме.
- ↑ Январь Линдстен: Нобелевские лекции по физиологии и медицине 1922-1941 гг. World Scientific, 1999, ISBN 981-02-3410-4 , стр. 119-152. ограниченный предварительный просмотр в поиске книг Google
- ↑ П. Мари, Ж. Клуне, Ж. Рауло-Лапуант: Вклад в развитие злокачественных опухолей на изъязвлениях Рентгена. В: Bulletin de l'AFEC. Том 8, 1910, с. 404-410.
- ↑ Йоханнес Фибигер (1867-1928) В: Ирландский журнал медицинских наук . Том 3, номер 3, 1928 г., стр. 129.
- ↑ Йоханнес Фибигер, доктор медицины В: Британский медицинский журнал. Том 1, номер 3500, февраль 1928 г., стр. 200, ISSN 0007-1447 . PMID 20773675 . PMC 2454517 (полный текст).
- ^ Нобелевская премия по физиологии и медицине 1926 - Йоханнес Фибигер. Источник : nobelprize.org , по состоянию на 23 марта 2013 г.
- ↑ Ф. Д. Баллок, Г. Л. Роденбург: Экспериментальная «карцинома» животных и их связь с истинными злокачественными опухолями. В: J Cancer Res . Том 3, 1918, стр. 227-240.
- ↑ П.Д. Столли, Т. Ласки: Иоганнес Фибигер и его Нобелевская премия за гипотезу о том, что червь вызывает рак желудка. В кн . : Анналы внутренней медицины . Volume 116, Number 9, May 1992, pp. 765-769, ISSN 0003-4819 . PMID 1558350 .
- ↑ Р. Д. Пасси, А. Лиз, Дж. К. Нокс: Рак Spiroptera и дефицит диеты. В кн . : Патология и бактериология . Том 40, 1935, с. 198-199.
- ↑ А.Л. Филдс, Д.Р. Сопрано, К.Дж. Сопрано: Ретиноиды в биологическом контроле и раке. В кн . : Журнал клеточной биохимии. Том 102, номер 4, ноябрь 2007 г., стр. 886-898, ISSN 0730-2312 . DOI: 10.1002 / jcb.21530 . PMID 17902161 . (Рассмотрение).
- ^ CR Hitchcock, ET Bell: Исследования паразитов нематод, Gongylonema neoplasticum (spiroptera neoplasticum) и авитаминоза А в лесном животе крыс: сравнение с результатами Фибигера. В: Журнал Национального института рака . Том 12, номер 6, июнь 1952 г., стр. 1345-1387, ISSN 0027-8874 . PMID 14939031 .
- ↑ Кристиан Н. Глуд: 100 дней для ознакомления с доказательной базой медицины: Fibigers kliniske forsøg med serumehandling af diffteri. Ugeskrift для Læger. Том 190, 1998, стр. 345-355. (Датский)
- ↑ HR Seibold, WS Bailey et al.: Наблюдения за возможной связью злокачественных опухолей пищевода и поражений Spirocerca lupi у собак. В: Американский журнал ветеринарных исследований . Том 16, номер 58, январь 1955 г., стр. 5-14, ISSN 0002-9645 . PMID 13228859 .
- ^ Р. Д. Мелендес, К. Суарес-Пеллин: Spirocerca lupi и собаки: роль нематод в канцерогенезе. В кн . : Тенденции паразитологии . Том 17, номер 11, ноябрь 2001 г., стр. 516; ISSN 1471-4922 . PMID 11872393 .
- ↑ Л.Л. ван дер Мерве, Р.М. Кирбергер и др.: Инфекция Spirocerca lupi у собак: обзор. В кн . : Ветеринарный журнал. Выпуск 176, номер 3, июнь 2008 г., стр. 294-309, ISSN 1090-0233 . DOI: 10.1016 / j.tvjl.2007.02.032 . PMID 17512766 . (Рассмотрение).
- ^ WS Bailey: Паразиты и рак: саркома у собак, связанная со спироцерка волчанкой. В: Анналы Нью-Йоркской академии наук . Том 108, ноябрь 1963 г., стр. 890-923, ISSN 0077-8923 . PMID 14081522 .
- ↑ Всемирная организация здравоохранения : Рак - Информационный бюллетень № 297 На: who.int от февраля 2012 г., по состоянию на 1 апреля 2013 г.
- ↑ Карл Генрих Бауэр: Мутационная теория развития опухоли. Шпрингер, Берлин, 1928 год.
- ↑ Йорг Р. Сиверт: Chirurgie, 7-е издание, Springer, 2001, ISBN 3-540-67409-8 , стр. 224. Ограниченный предварительный просмотр в поиске книг Google
- ↑ Тамара Лебедева: Канцерогены открыты! 4-е издание, Дриедигер, 2002 г., ISBN 3-932130-13-8 .
- ↑ HR Clark: Лечение и профилактика всех видов рака: революционный метод лечения рака. Доктор Центр Кларка, 2010, ISBN 0-9740287-9-7