Окисление парафина

Парафина к окислению является историческим химико-промышленным способом производства синтетических жирных кислот , содержащих в химическую промышленность как для потребительских товаров , таких как мыла и пищевых жиры и смазки , обработанных для технических применений. Также был произведен широкий спектр карбоновых кислот и продуктов окисления, таких как спирты , альдегиды , сложные эфиры и кетоны . В качестве сырья использовался парафиновый шлам , полученный из угля, смесь насыщенных высокомолекулярных углеводородов и побочный продукт синтеза Фишера-Тропша . Парафины окисляли в жидком состоянии молекулярным кислородом воздуха с разрывом углеродной цепи в присутствии перманганатов при температурах в диапазоне от примерно 100 до 120 ° C и при нормальном давлении .
Продукты окисления парафинов конкурировали с встречающимися в природе жирными кислотами. Нехватка из-за конфликтов или узких мест в поставках продуктов питания повысила интерес к синтетическим жирным кислотам. В Германии этот процесс получил коммерческое значение с середины 1930-х годов в рамках усилий самодостаточность в Германской империи и не проводили в промышленном масштабе , пока первые годы после Второй мировой войны . Этот процесс использовался для производства сырья для сектора технических жиров и моющих средств ; нативные жиры, ранее необходимые для этого, теперь доступны для пищевой промышленности. Более того, в то время сенсацией считалось крупномасштабное производство искусственных жиров, пригодных для употребления в пищу человеком («сливочного масла») из угля , которое стало возможным впервые благодаря окислению парафина .
Из-за высокой доступности недорогих природных жиров и конкуренции со стороны жирных спиртов на основе нефти , этот процесс потерял свое значение в западном мире в начале 1950-х годов. Варианты процесса, такие как окисление Башкирова, при котором алканы окисляются до вторичных спиртов в присутствии борной кислоты без разрыва цепи , все еще используются в химической промышленности для специальных синтезов, например, для производства циклододеканола .
сказка

Ранняя работа
Парафины представляют собой смесь алканов , предельных углеводородов с общей эмпирической формулой C n H 2n + 2 . Его название происходит от латинского parum affinis , мало вовлеченного . Парафины считались не очень реактивными; например, с восстановителями, такими как металлический натрий , парафины не вступают в реакцию при температуре окружающей среды.
В 1854 году, всего через 19 лет после открытия парафинов Карлом фон Райхенбахом , Готтхард Хофштадтер указал, что парафины не так инертны, как предполагает их название. Он впервые сообщил о попытках окислить парафины путем кипячения их с азотной кислотой . Основными продуктами, которые он получил, были янтарная кислота , дикарбоновая кислота и низкомолекулярные водорастворимые монокарбоновые кислоты . Другие сильные окислители, такие как хромовая кислота, которую использовал Эдуард Мейсель , также приводили к образованию карбоновых кислот. В 1874 году А.Г. Пуше описал окисление парафинов с использованием смеси дымящей азотной и серной кислоты при температурах ниже 110 ° C. В качестве продуктов снова был получен ряд низкомолекулярных водорастворимых карбоновых кислот. Кроме того, Пуше впервые идентифицировал новую карбоновую кислоту с более высоким молекулярным весом, жирную кислоту, которую он назвал «парафиновой кислотой ».
Окисление воздухом
Помпеж Болли признал в 1868 году, что парафины поглощают кислород воздуха при температуре 150 ° C, Карл Энглер обнаружил образование водорастворимых жирных кислот в аналогичных исследованиях в 1879 году. Однако исследователи не осознавали практического значения своих наблюдений. Лишь несколько лет спустя Ойген Шааль осознал коммерческий потенциал этой реакции. В 1884 году он подал первый патент на превращение нефти и подобных углеводородов в карбоновые кислоты окислением воздухом. Среди прочего, Шаал использовал в качестве катализатора хлораты , перманганаты и нитраты, адсорбированные на кизельгуре . Использование недорогого атмосферного кислорода представляло собой значительный прогресс на пути к технической реализации процесса.Поскольку жирные кислоты из природных источников были в достаточной степени доступны до начала Первой мировой войны , коммерциализация этих процессов изначально не имела смысла.
Это было только тогда , когда жиры и жирные кислоты , таким образом , стали редкими во время мировой войны , что химическая промышленность активизировали научные усилия для того , чтобы по крайней мере , получить сырье для производства мыла , основанный на нефти или дегтя от тлеющих из бурого угля . Попытки перенести уже известные на тот момент процессы в промышленную практику увенчались успехом лишь частично. Первый технический процесс во время войны был осуществлен компанией Fanto в Пардубице, и в качестве катализатора использовалась соль ртути . Однако полученные жирные кислоты были плохого качества, и на преобразование парафинов уходили дни. Улучшение выхода и качества было достигнуто благодаря систематическому исследованию влияния температуры и количества воздуха на качество продукта окисления Адольфом Грюном из Shift AG . Жирные кислоты, технически производимые Layer AG, могли хорошо омыляться, мыла обеспечивали удовлетворительный моющий эффект.
После Первой мировой войны в 1920-х годах более крупные химические компании, такие как IG Farben и Henkel и Hubbe & Fahrenholz, в то время одна из крупнейших и наиболее важных нефтедобывающих фабрик в Германии, продолжали исследования в области окисления парафина. Производственное предприятие IG Farben в Людвигсхафене начало производство синтетических жирных кислот в меньшем масштабе с 1928 года, совместное предприятие IG Farben и Standard Oil of New Jersey в Батон-Руж в 1931 году производило около 3 тонн жирных кислот в день на основе парафинов, полученных из нефти. Однако жирные кислоты, полученные в процессе, привели к получению мыла низкого качества с проблемами запаха при дальнейшей обработке. Поскольку парафинов было мало и поэтому они были дорогостоящими, способ не давал никаких экономических преимуществ по сравнению с затратами на приобретение природных жирных кислот на тот момент.
Немецкие жирные кислоты работают
Коллоидный химик Артур Imhausen , совладелец в мыловаренной промышленности Märkische , возобновил исследование Eugen Schaal в 1930 - х годах. Вместе со своим коллегой Вернером Прошем он разработал процесс Имхаузена-Проша для окисления парафина. В процессе использовался воздух в качестве окислителя и перманганат калия в качестве инициатора. Первоначально Имхаузен использовал парафины от гидрирования продуктов карбонизации бурого угля. Комиссар по экономическим вопросам Вильгельм Кепплер , который отвечал как за реализацию четырехлетнего плана с акцентом на «промышленные жиры и масла», так и за продвижение производства бензина, предложил Имхаузену использовать парафиновый гач из синтеза Фишера-Тропша в качестве сырья. . Гач представлял собой смесь алканов без значительных примесей, которую до этого считали разрушительным побочным продуктом синтеза Фишера-Тропша. Оказалось, что это идеальное сырье для окисления парафинов. Поскольку в синтезе Фишера-Тропша можно использовать все типы угля, для производства сусла существовала широкая сырьевая база. Кроме того, империя приняла на себя ценовые гарантии на поставляемое сырье, а также на производимые жирные кислоты.
Что касается парафина гач, Имхаузен добился выхода целевых продуктов - основных жирных кислот с длиной цепи от 11 до 20 атомов углерода - около 50%. У Имхаузена не было необходимого капитала для крупномасштабной реализации, и возникли технические проблемы с переработкой сырой смеси жирных кислот. Поскольку компания Henkel также интересовалась жирными кислотами и располагала достаточными финансовыми ресурсами, Имхаузен и Хенкель основали Deutsche Fettäur-Werke GmbH в Виттене 21 февраля 1936 года как совместное предприятие по производству и сбыту жирных кислот с использованием процесса Имхаузена-Прош. Акционеры назначили Артура Имхаузена и Эриха Грюнталя управляющими директорами, а председателем наблюдательного совета стал изобретатель Persil Хуго Хенкель .
Поскольку IG Farben также разработала процесс окисления парафинов, Keppler инициировал сотрудничество между немецким заводом по производству жирных кислот и IG Farben с целью оптимизации производственных процессов. Процесс IG Farben дает преимущества при дальнейшей переработке сырых жирных кислот. Примерно с мая 1938 года Имхаузен преодолел технические трудности обработки сырых жирных кислот с помощью процесса IG Farben и получил высококачественный продукт. Поскольку топливо Фишера-Тропша имело низкое октановое число , национал-социалистические экономические лидеры вместо этого построили больше установок гидрогенизации на основе процесса Бергиуса-Пьера , который обеспечивал более качественный автомобильный бензин ; Получить гачу стало трудно. Лишь в 1940 году заводы Фишера-Тропша значительно увеличили свою производительность, что привело к хорошему запасу шлама. По инициативе Имхаузена Кепплер перевел системы Фишера-Тропша на процесс среднего давления , что обеспечило более высокий выход парафина. Заводы IG Farben в Людвигсхафен-Оппа и Хейдебрек производили по 20 000 тонн каждый, а завод Witten - 40 000 тонн жирных кислот в год. В то время как завод Виттен обрабатываются почти исключительно Фишера-Тропша-Gatsch, завод Oppau потребляется около 80% лигнита на основе TTH парафины, 10% Фишера-Тропша-Gatsch и 10% Nerag-Gatsch, поступившие от снижения из температура застывания от шпинделя масла .
Масло угольное

До начала Второй мировой войны внутреннее производство в Германии удовлетворяло менее половины потребности в диетических жирах, составлявшей около 1,6 миллиона тонн, в техническом секторе с потребностью около 400 000 тонн лишь около 13%. Германия покрыла оставшуюся потребность путем импорта масел и жиров из масличных растений из Восточной Азии и Южной Америки , а также арктических китов масел . Политическое намерение положить конец зависимости Германского рейха от импорта технических жиров и диетических жиров вскоре привело к так называемому жировому разрыву . С августа 1939 года, за четыре дня до начала войны, национал-социалисты нормировали закупку жиров и контролировали их выпуск с помощью толстой карты Рейха .
Артур Imhausen, который был еврейского происхождения, удалось производить первый синтетический съедобного жира в мире из чистых жирных кислот из парафина окисления путем этерификации с глицерином, тем самым поддерживая усилия Третьего рейха , чтобы стать самодостаточным. По предложению Германа Геринга , Адольф Гитлер тогда признал семью Imhausen в качестве арийцев . С 1941 года Deutsche Fettwerke Witten производила 250 тонн искусственного пищевого жира в месяц на большом предприятии. По совету Вильгельма Кеплера, национал - социалисты распространяли синтетические смазки на экспериментальной основе в течение примерно трех лет , заключенные в концлагере Заксенхаузен и в лагерях трудовой повинности рейха в Trebbin и Ruhlsdorf. Врачи из физиологического департамента Рейхского управления здравоохранения также проводили эксперименты по кормлению животных. Наличие нечетных жирных кислот, которые редко встречаются в нативных жирах, считалось поводом для беспокойства. Однако отрицательные физиологические эффекты продемонстрировать не удалось. С другой стороны, пропорции этил-разветвленных карбоновых кислот в жире, так называемых изожирных кислот, приводят к образованию дикарбоновых кислот, которые вредны для здоровья и которые могут быть обнаружены в моче даже после небольшой дозы. После трех лет испытаний в 1939 году, через несколько дней после нападения немецкого вермахта на Польшу , Имперское управление здравоохранения оказалось под политическим давлением, и искусство употребления масла в пищу было бесплатным. Жир служил добавкой к тяжелому рабочему пайку, к столовой в больницах, а также к пайку узников трудовых и концлагерей и советских военнопленных . Во время африканской кампании и на немецких подводных лодках военные снабжали солдат пищевым жиром производства Виттена. Жир почти не прогоркнул из-за высокого содержания насыщенных жирных кислот и, следовательно, оставался долговечным. По вкусовым качествам он был близок к маслу и имел такую же теплотворную способность . Надежды Имхаузена на объем производства более 100 000 тонн в год не оправдались, однако во время войны немецкие заводы по производству жирных кислот производили только около 3 000 тонн в год.
послевоенный период

К концу Второй мировой войны и в первые послевоенные годы запасы жира резко сократились. В 1947 году годовое потребление на душу населения в Германии, составлявшее в 1938 году 25,6 килограмма, упало до 5,7 килограмма. Политики и промышленники пытались стимулировать импорт жира и получить разрешение на возобновление синтеза Фишера-Тропша и процесса Имхаузена-Проша. Производственные мощности Немецкого завода по производству жирных кислот имели производственную мощность около 600 тонн синтетического масла в месяц. Кроме того, использование синтетических жирных кислот в технических целях высвободило такое же количество природных жирных кислот для пищевых целей. Процесс Имхаузена-Проша требовал семи тонн угля на тонну масла; Чтобы иметь возможность импортировать такое же количество масла, в послевоенный период потребовалась выручка от продаж, в десять раз превышающая объем угля на мировом рынке .
Сыну Артура Имхаузена, Карлу-Хайнцу Имхаузену, удалось ненадолго возобновить производство мыла и жиров на основе углерода в послевоенный период: в 1946 году завод Виттена производил около 350 тонн синтетического жира в месяц. Но интерес к окислению парафинов и углеродистым жирным кислотам закончился в 1950-х годах с наступлением экономического чуда . Внезапный избыток натуральных жиров на мировом рынке привел к резкому падению цен на жиры и жирные кислоты. На рынке поверхностно-активных веществ жирные кислоты, полученные из углерода, конкурировали как с олеохимическими, так и с нефтехимическими продуктами, такими как спирты Циглера . Хотя этот процесс больше не был конкурентоспособным в западном мире, и жирные кислоты практически не производились искусственно, их продолжали производить в Советском Союзе и Китае . В 1978 году, например, в Советском Союзе и Китае более 500 000 тонн жирных кислот были получены из парафина и керосина путем окисления на марганцевых катализаторах.
сырье
Парафины, используемые при окислении, имеют длину углеродной цепи примерно от 18 до 30 атомов углерода, что соответствует интервалу плавления от 28 до 66 ° C и интервалу кипения от 320 до 460 ° C. Целевые продукты, жирные кислоты с длиной цепи от 10 до 18 атомов углерода, могут быть получены с максимальным выходом из парафинов этого диапазона длин цепей. Парафины должны иметь как можно более прямую цепочку для достижения высокого качества продукта. Мыло с разветвленной жирной кислотой было плохим моющим средством и имело характерный запах. В случае разветвленных парафинов кислород также предпочтительно атакует третичный атом водорода. Хотя образуются жирные кислоты с прямой цепью, они содержат непропорционально большую долю низкомолекулярных жирных кислот.
Парафины получали в основном в результате двух процессов: гидрирования лигнита и его обуглившихся смол под высоким давлением и синтеза Фишера-Тропша. В процессе гидрогенизации при низкой температуре и высоком давлении получаются так называемые парафины TTH с прямой цепью со степенью разветвления от 10 до 15%. Хотя бурый уголь был доступен в больших количествах, проблемы со сбытом побочных продуктов карбонизации привели только к относительно низкой доступности подходящих парафинов из этого источника. Кроме того, н-алканы в результате из мочевины экстрактивной кристаллизации из смазочных масел , также пригодны в качестве сырья.
В процессе синтеза Фишера-Тропша при низком давлении был получен гач с правильным распределением длины углеродной цепи. Промежуток от процесса среднего давления был более подходящим, потому что он был особенно линейным, но все же содержал от 15 до 20% короткоцепочечных разветвленных парафинов. Благодаря наличию в них третичных атомов водорода, которые легче поддаются окислительной атаке, они особенно подходят в качестве исходного материала для окисления парафинов. Кроме того, выход целевых парафинов в процессе среднего давления был примерно в четыре-пять раз выше, чем в процессе низкого давления. Вместо этого диапазон длин цепи был смещен в сторону более длинных цепей, что потребовало получения осадка путем перегонки.
Из-за их ингибирующего действия предел содержания серосодержащих соединений и фенолов составлял 0,05%. Гидрированием сырья удаляются деструктивные олефины и кислородсодержащие соединения. Нефть вряд ли подходила в качестве сырья для окисления парафинов из-за содержания в ней нафтенов , что приводило к образованию вязких жирных кислот плохого моющего качества. Длинноцепочечные разветвленные парафины, олефины и нафтены также приводят к более высокому содержанию нежелательных гидроксикарбоновых кислот при окислении . Пригодность парафина проверялась испытанием на окисление.
Процедура
Процесс состоял из трех основных стадий окисления, переработки окислительной смеси в сырые жирные кислоты и, наконец, их разделения дистилляцией на фракции жирных кислот. Химическая промышленность далее перерабатывала фракции жирных кислот в конечные продукты, такие как мыло, детергенты , пластификаторы и синтетический жир. Операторы проводили окисление парафина почти исключительно в периодическом режиме , то есть прерывисто.
окисление
Окисление было важной стадией процесса. Парафин реагировал в жидком состоянии при минимально возможных температурах и в присутствии катализатора с атмосферным кислородом в течение примерно 15-30 часов, пока примерно 30-50% парафина не превратилось в жирную кислоту. Это сводило к минимуму образование нежелательных побочных продуктов, таких как пропорции дикарбоновых кислот, гидроксикарбоновых кислот и низкомолекулярных жирных кислот, которые нерастворимы в петролейном эфире.
После короткой латентной фазы, типичной для автокаталитических реакций, начинается окисление, о чем свидетельствует образование воды и увеличение кислотного числа продукта. Если сырье содержало ингибиторы , их сначала нужно было окислить, прежде чем реакция могла начаться. С другой стороны, присутствие циклических и ненасыщенных углеводородов приводит к образованию ингибиторов, которые подавляют реакцию, которая уже началась, или останавливает ее. Реакция схематично протекала по общему уравнению:
Образовавшиеся жирные кислоты все еще подвергались постокислению, так что образовывалось избыточное количество низкомолекулярных жирных кислот по сравнению со статистически ожидаемым распределением. Жирные кислоты, спирты, альдегиды, кетоны, сложные эфиры и лактоны образовывались как нелетучие продукты, тогда как диоксид углерода , вода, низкомолекулярные карбоновые кислоты и их сложные эфиры, а также пероксиды, альдегиды и спирты образовывались как летучие продукты .
Давление и температура
Высокое реакционное давление увеличивает долю кислорода, растворенного в парафине, и, следовательно, скорость реакции. Увеличение давления вдвое сократило время реакции примерно вдвое. Во время Второй мировой войны Hubbe & Fahrenholz построили в Магдебурге завод, который должен был работать при давлении 25 бар и без катализатора. Однако компания больше не ввела систему в эксплуатацию. Все остальные системы работали при нормальном давлении. Содержание растворенного кислорода увеличивается за счет тонкодисперсного барботирования воздуха, например, через фильтрующие свечи или наполнители .
При температурах выше 170-180 ° C окисление протекало довольно быстро, но образовывались переокисленные продукты, непригодные для дальнейшей переработки в поверхностно-активные вещества. Относительно низкая температура окисления является преимуществом для получения чистых жирных кислот. При ограничении оборота около 30% и температуре от 105 до 120 ° C химическая промышленность получала жирные кислоты с высокой селективностью и хорошим качеством. Время реакции, которое было слишком большим для промышленных целей, привело к необходимости использования катализатора.
Катализатор / инициатор

Катализаторы, используемые для окисления парафинов, варьировали. Часто это были оксиды металлов подгруппы, такие как соли кобальта . Перманганат калия оказался хорошим инициатором окисления парафинов . Соли щелочных металлов действовали как сокатализаторы, которые добавляли в процесс через мыльные компоненты обработанных и переработанных парафинов.
Суспензия перманганата калия в парафинах была создана путем добавления и быстрого перемешивания концентрированного водного раствора перманганата. При температуре выше 100 ° C вода испарялась и осталась тонкодисперсная суспензия инициатора. Используемое количество составляло приблизительно от 0,1 до 0,3% от количества используемого парафина и варьировалось в зависимости от качества исходного материала. Добавив катализатор, операторы достигли целевой конверсии около 30% после времени реакции от 10 до 15 часов при относительно низких температурах от 110 до 120 ° C. Низкая температура реакции подавляла образование нежелательных побочных продуктов, таких как гидроксильные или дикарбоновые кислоты, и цвет продукта улучшался.
Ведение производства
Парафина окисление проводят в кислотостойких стальных или алюминиевых реакторов. Они имели диаметр 1–3 метра и высоту 8–12 метров. Воздух барботировал через фильтрующие пластины или свечи, воздух распределялся в реакторе через насадку. Летучие кислоты и побочные продукты растворяются в промывной машине, наполненной водой. Для окисления тонны парафина требовалось около 50 кубометров воздуха в час. Для начала реакции изначально требовалась температура около 150 ° C. После того, как реакция началась, примерно через 20-60 минут температуру реакции снизили до ниже 120 ° С. Избыточный воздух уносил низкомолекулярные компоненты. О начале реакции свидетельствует накопление воды в конденсаторе , в котором также собираются летучие продукты окисления.
Поскольку окисление было экзотермическим , реактор необходимо было охладить. Количество выделяющегося тепла соответствует примерно 4,5% теплоты сгорания парафина на тонну продукта окисления примерно 2100 мегаджоулей . Если было достигнуто кислотное число 70, это означало, что целевая конверсия была достигнута и окисление можно было прекратить. Тогда конверсия составила около 30%. Лимит продаж снизил образование побочных продуктов жирных кислот, таких как гидроксикарбоновые кислоты и дикарбоновые кислоты.
Обработка сырых жирных кислот
Неочищенные жирные кислоты содержали смесь карбоновых кислот со всеми длинами цепей, содержащихся в используемом парафине, непревращенный парафин и широкий спектр продуктов окисления. При обработке жирные кислоты, содержащиеся в продукте окисления, сначала промывали водой, чтобы отделить низкомолекулярные кислотные компоненты и катализатор.
Чтобы отделить жирные кислоты от неомыляемых фракций, неочищенный оксидат сначала нейтрализовали гидроксидом натрия с образованием мыла. Образующиеся сложные эфиры также омыляются при более высоких температурах. Затем неомыляемые фракции смешивали с 45-процентным этанолом или 20-процентным 2-пропанолом в сосуде с мешалкой . Мыло растворялось в спирте, а неомыляемые фракции осаждались в виде масляного слоя на спиртово-мыльной смеси. Масляный слой, который в основном содержит парафины и назывался неомыляемым I (УФ I) , был возвращен в процесс окисления. Доля УФ I в общей доле неомыляемых компонентов составляла около 85%.
Оставшиеся неомыляемые части, называемые неомыляемыми II (УФ II) , содержат, помимо остатков парафинов, прежде всего, все продукты окисления, такие как спирты, сложные эфиры и лактоны. Операторы растений удаляют эти компоненты путем экстракции с бензином в противотоке. UV II и бензин разделяли перегонкой . После того как спиртовая и мыльная фазы были разделены перегонкой, последним этапом было извлечение жирных кислот путем их подкисления минеральными кислотами, такими как серная или соляная кислота . Остатки короткоцепочечных карбоновых кислот удаляли промыванием водой. Затем с помощью вакуумной перегонки с водяным паром жирные кислоты были разделены на отдельные фракции.
Продукты
Основные жирные кислоты с длиной углеродной цепи примерно от 10 до 20 атомов углерода нейтрализовали каустической содой для получения мыла. В отличие от природных жирных кислот синтетические жирные кислоты содержат доли нечетных углеродных цепей. Моющие свойства мыла, полученного таким образом, не отличались от мыла из местных источников. Присутствие неомыляемых фракций, присутствие лактонов и присутствие жирных кислот с разветвленной цепью частично приводило к проблемам с запахом. Гидрирования уменьшило жирных кислот с жирными спиртами. По сульфатации с триоксида серы вышел из жирных спиртов, сульфаты жирных спиртов.
Имхаузен был первым, кто начал производить жиры в промышленных масштабах путем этерификации глицерином, а затем начал производить масло из синтетических жирных кислот путем эмульгирования . Для этого в жирной кислоте работает только натуральный глицерин из непищевых жиров. Синтетический глицерин, производимый IG Farben в Хейдебреке, оказался недостаточно чистым для этой цели. Жирные кислоты этерифицируются стехиометрическим количеством глицерина с использованием цинковой пыли . После завершения реакции обработка 20-процентной серной кислотой растворила цинк. После нейтрализации раствором гидроксида натрия следы мыла удаляли смесью активированного угля и фуллеровой земли. Имхаузен получил путем вакуумной перегонки чистый жир, пригодный для употребления.
Первоначально жирные кислоты восстанавливались до спирта и перерабатывались в пластификаторы после этерификации фталевым ангидридом или другими ангидридами. Операторы вернули оставшиеся жирные кислоты с более высокой молярной массой в процесс окисления. Конденсат воздухоохладителя содержал около 80% муравьиной кислоты и 9% уксусной кислоты и использовался для консервирования кормов для скота. В лакокрасочной промышленности в качестве связующего для пигментов использовались остатки от перегонки жирных кислот.
механизм
Первый подход к объяснению окисления парафиновых углеводородов был предоставлен теорией перекиси, разработанной Алексеем Николаевичем Бахом и Карлом Энглером, которая известна как теория Энглера-Баха. Соответственно, во время окисления на первой стадии образуется вторичный гидропероксид . Эта теория, согласно которой этот гидропероксид затем радикально разлагается, была позже подтверждена Эриком Ридалом .
Функция металлического катализатора заключается в увеличении скорости как образования, так и разложения этого гидропероксида. Среди прочего, это создает алкильный радикал, который реагирует с кислородом с образованием пероксорадикала . Это образует новый алкильный радикал и гидропероксид , отделяя атом водорода от другой молекулы парафина.
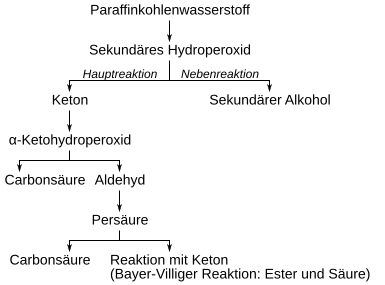
Соли щелочных металлов также разлагают пероксиды и вступают в реакцию в качестве сокатализатора. Относительная скорость атаки кислорода на первичные, вторичные и третичные атомы водорода составляет примерно 1: 3: 33. Атака на преимущественно встречающиеся вторичные атомы водорода является чисто статистической и приводит к образованию почти эквимолярной смеси всех теоретически возможных карбоновых кислот. Из-за большого количества образующихся продуктов точное объяснение механизма реакции оказалось затруднительным. Последовательность реакций окисления и образования основных и побочных продуктов лучше всего объясняется схемой, разработанной Вольфгангом Лангенбеком и Вильгельмом Прицковым :
Первая стадия - это гидропероксид, который в ходе основной реакции распадается на воду и кетон . Вторичные спирты образуются в качестве побочной реакции по следующей схеме реакции:
Кетон подвергается дальнейшему окислению. Метиленовая группа предпочтительно окисляется в α-положении до кетогруппы. Образующийся α-кетогидропероксид распадается на альдегид и карбоновую кислоту с перегруппировкой .
Прицков использовал циклогексанон в качестве модельного вещества и тем самым показал правильность модельной концепции. Альдегид превращается в карбоновую кислоту на стадии пероксикарбоновой кислоты и последующей реакции с другим альдегидом. Образование сложных эфиров карбоновой кислоты и других карбоновых кислот происходит посредством окисления кетона по Байеру-Виллигеру пероксикарбоновой кислотой в соответствии со следующим уравнением:
Другая возможная реакция α-кетогидропероксидов - образование дикетонов .
Они реагируют с пероксикарбоновыми кислотами с образованием ангидридов кислот и карбоновых кислот.
Башкировское окисление
Если окисление парафина проводится в присутствии борной кислоты , вторичные жирные спирты являются основным продуктом . Этот процесс получил название окисления Башкирова в честь его первооткрывателя Андрея Николаевича Башкирова, который разработал процесс в 1950-х годах. Окисление Башкирова не разрушает исходный парафин; длина цепи получаемых спиртов соответствует длине цепи парафинов, используемых в качестве сырья. Длины цепей исходных парафинов соответственно короче по сравнению с длинами цепей, используемых при окислении парафинов.
Процесс проводят при температуре от 150 до 160 ° C, при содержании перманганата калия 0,1% в качестве инициатора и около 5% борной кислоты . Борная кислота улавливает образующиеся гидропероксиды и превращает их в их сложные эфиры, нечувствительные к дальнейшему окислению. Последующий гидролиз сложного эфира дает вторичные спирты, которые превращаются во вторичные алкилсульфаты или оксид этилена с образованием неионных поверхностно-активных веществ . Для сдерживания побочных реакций конверсия ограничивается примерно 20%, содержание кислорода в воздухе снижается до 3,5% за счет разбавления азотом. В этом процессе конверсию можно контролировать с помощью инфракрасного анализа по интенсивности поглощения бор-кислородного валентного колебания боратного воска. Окисление Башкирова используется в специальных процессах, например, при производстве циклододеканона . В этом процессе циклододеканол получают путем окисления циклододекана кислородом воздуха , который затем дегидратируется до циклододеканона.
литература
- Фридрих Асингер : Химия и технология парафиновых углеводородов . Академия Верлаг, 1956.
- Вильгельм Кейм , Арно Бер , Гюнтер Шмитт: Основы промышленной химии. Отто Салле Верлаг, 1985, ISBN 3-7935-5490-2 .
- Клаус Вайссермель , Ханс-Юрген Арпе : Промышленная органическая химия: важные предварительные и промежуточные продукты. Wiley-VCH, 2007, ISBN 978-3-527-31540-6 .
- Биргит Пельцер-Райт и Рейнхольд Райт : «Жир из угля»? Синтез пищевых жиров в Германии 1933-1945 гг . В: Technikgeschichte , Vol. 69 (2002), H. 3, pp. 173–205.
веб ссылки
- Welt im Film 121/1947 - 19 сентября 1947 г. (с 2:40 до 4:20 мин.) , Жир из угля, кинохроника 1947 года о производстве масла и мыла в Deutsche Fettsäurewerke
Индивидуальные доказательства
- ↑ Карл Фрайхер фон Райхенбах, Франц Вильгельм Швайггер-Зайдель: Креозот в химическом, физическом и медицинском отношении . 2-е, предположительно издание, Лейпциг, Барт 1835 г.
- ↑ П. Готтхард Хофштадтер: Об искусственном и минеральном парафине. В кн . : Анналы химии и фармации . 91, 1854, стр. 326-334, DOI : 10.1002 / jlac.18540910307 .
- ↑ CH Gill, Ed. Мейсель: XLI. О парафине и продуктах его окисления. В: Журнал химического общества . 21, 1868, стр. 466, DOI: 10.1039 / JS8682100466 .
- ^ AG Pouchet: Влияние азотной кислоты на парафин. В: Политехнический журнал . 214, 1874, с. 130-132.
- ↑ П. Болли: О некоторых новых свойствах парафина и о парафиновых ваннах. В: Политехнический журнал . 190, 1868, стр. 121–124.
- ↑ К. Энглер, Дж. Бок, Бер. Немецкая хим. Ges. , 1879, 12, с. 2186.
- ↑ Патент US335962 : Преобразование нефти и подобных углеводородов в кислоты. Опубликовано 9 февраля 1886 г. , изобретатель: Ойген Шааль.
- ↑ a b c d e f g Артур Имхаузен: Синтез жирных кислот и его важность для обеспечения немецких жировых запасов. В кн . : Коллоидный журнал . 103, 1943, стр. 105-108, DOI: 10.1007 / BF01502087 .
- ^ Адольф Грюн: окисление парафина. В: Отчеты Немецкого химического общества (серии A и B). 53, 1920, стр. 987-996, DOI: 10.1002 / cber.19200530618 .
- ^ A b c Фридрих Азингер: Химия и технология парафиновых углеводородов . Академия Верлаг, 1956, с. 491–493.
- ↑ a b c d Бернд Кайзер: Значение рамочных условий экономической политики для закупок сырья международными промышленными компаниями и вытекающие из этого корпоративные стратегии на примере Группы Хенкель . Вступительная диссертация на получение ученой степени доктора экономических и социальных наук (Dr. rer. Pol.) В Университете Фридриха Александра в Эрлангене-Нюрнберге, 2009 г., стр. 142–154. ( PDF )
- ↑ a b c d Ральф Кляйн: Артур Имхаузен (1885–1951) . В: Вольфганг Вебер (Hrsg.): Инженеры из Рурской области (= Rheinisch-Westfälische Wirtschaftsbiografien ). лента 17 . Aschendorfer Verlagsbuchhandlung GmbH, Мюнстер 1999, ISBN 3-402-06753-6 , стр. 344-372 .
- ^ A b Карл Т. Зильч: Синтетические жирные кислоты в Восточной Европе. В: Журнал Американского общества химиков-нефтяников . 45, 1968, стр. 11, DOI: 10.1007 / BF02679036 .
- ↑ a b c d e f Синтетические жирные кислоты и детергенты. В: Заключительный отчет BIOS No. 1722, поз. 22. Архивировано из оригинала апреля 2, 2015 ; Доступ к 14 марта 2015 года .
- ↑ а б в г д Биргит Пельцер-Райт, Рейнхольд Райт : «Жир из угля»? Синтез пищевых жиров в Германии 1933–1945 гг . В: Technikgeschichte , 69, 2002, стр. 173–206.
- ↑ Майкл Вильдт: Мечта о сытости. Гамбург 1986, ISBN 3-87975-379-2 , стр.17 .
- ↑ Бруно Фишер: Рурская область 1933–1945 гг. Исторический путеводитель . Ch. Links Verlag, 2009, ISBN 978-3-86153-552-2 , стр. 86.
- ↑ Беренд Штральманн: Имхаузен, Артур. В: Новая немецкая биография (NDB). Том 10, Duncker & Humblot, Берлин 1974, ISBN 3-428-00191-5 , стр. 145 f. ( Оцифрованная версия ).
- ↑ Ричард Брайтман: Архитектор «окончательного решения». Генрих Гиммлер и истребление европейских евреев. Падерборн 1996, стр. 52-53.
- ^ Х. Краут: физиологическая ценность синтетических жиров. В: Британский журнал питания . 3, 1949, с. 355, DOI: 10.1079 / BJN19490049 .
- ↑ a b Ганс Генрих Майер-Деринг: Безопасно ли использование синтетических жирных кислот для пищевых продуктов? В: Клинический еженедельник . 27, 1949, стр.113, DOI: 10.1007 / BF01471275 .
- ↑ а б в Двадцать минут воровства угля, но двойная фильтрация жира . В: Der Spiegel . Нет. 49 , 1947, стр. 6 ( онлайн ).
- ^ W. Heimann: Fette und Lipoide , Springer Verlag, 1969, ISBN 978-3-642-46190-3 , стр. 7.
- ^ JW Винсент: Аспекты синтетических жирных кислот и синтетических жиров в Германии. В: Заключительный отчет BIOS. 805, 1946. 1946, архивируются с оригинала апреля 2, 2015 ; Доступ к 18 марта 2015 года .
- ↑ Триумф нефтяников . В: Der Spiegel . Нет. 31 , 1952, стр. 10-11 ( онлайн ).
- ^ Х. Файнберг: Синтетические жирные кислоты. В: Журнал Американского общества химиков нефти. 56, 1979, стр. 805A, DOI : 10.1007 / BF02667451 .
- ↑ a b c d e f Фридрих Азингер: Химия и технология парафиновых углеводородов . Академия Верлаг, 1956, с. 493-497.
- ^ Вильгельм Кейм, Арно Бер и Гюнтер Шмитт: Основы промышленной химии. Технические продукты и процессы, Отто Салле Верлаг, 1985, ISBN 3-7935-5490-2 , с. 250.
- ↑ а б в г д Г. Витцель: Производство синтетических жирных кислот путем окисления парафиновых углеводородов молекулярным кислородом. В кн . : Химическая инженерия . 3, 1954, стр. 17-IN4, DOI : 10.1016 / S0009-2509 (54) 80003-0 .
- ↑ a b c d Фридрих Азингер: Химия и технология парафиновых углеводородов . Академия Верлаг, 1956, с. 498-499.
- ^ Фрэнсис Фрэнсис, Уолтер Фредерик Миллард и а .: XLVI - Скорость окисления парафина. Части I-IV. В: Journal of the Chemical Society, Transactions . 125, 1924, стр. 381, DOI: 10.1039 / CT9242500381 .
- ^ Фридрих Асингер: Химия и технология парафиновых углеводородов . Академия Верлаг, 1956, с. 478-490.
- ^ Фридрих Асингер: Химия и технология парафиновых углеводородов . Академия Верлаг, 1956, с. 502–503.
- ↑ Патент DE739570 : Процесс производства продуктов окисления, таких как жирные кислоты или спирты, путем окисления углеводородов. Опубликовано 12 августа 1943 г. , изобретатель: Карл Бласс.
- ^ A b c Фридрих Азингер: Химия и технология парафиновых углеводородов . Академия Верлаг, 1956, с. 500–502.
- ↑ Патент US2249708 : Метод окисления парафина. Опубликовано 15 июля 1941 г. , изобретатель: Милдред М. Хикс-Бруун.
- ^ NM Emanuel ': Окисление углеводородов в жидкой фазе. Elsevier, 2013, ISBN 978-1-4831-4925-7 , стр. 324 ( ограниченный предварительный просмотр в поиске книг Google).
- ↑ a b c d Фридрих Азингер: Химия и технология парафиновых углеводородов . Академия Верлаг, 1956, с. 504–508.
- ↑ a b c d e Фридрих Азингер: Химия и технология парафиновых углеводородов . Академия Верлаг, 1956, с. 508-513.
- ↑ Людвиг Маннес: О побочных продуктах окисления парафина. В кн . : Химия . 57, 1944, стр. 6, DOI: 10.1002 / ange.19440570102 .
- ^ К. Энглер, В. Уайлд: О так называемой активации кислорода и об образовании супероксида. В: Отчеты Немецкого химического общества . 30, 1897, стр. 1669, DOI: 10.1002 / cber.18970300295 .
- ↑ А. Н. Бах: О роли перекисей в процессах медленного окисления. В: Ж. Сажа. Phys-Chem. Soc. , 29, 1897, стр. 373-395.
- ^ П. Джордж, EK Rideal, A. Робертсон: Окисление жидких углеводородов. I. Цепное образование гидропероксидов и их разложение. В: Proceedings of the Royal Society A: Mathematical, Physical and Engineering Sciences. 185, 1946, с. 288, DOI: 10.1098 / rspa.1946.0019 .
- ↑ В. Лангенбек, В. Прицков: Исследования механизма окисления парафинов, 1-я часть. В: жиры, мыло, краски . 55, 1953, стр. 435, DOI: 10.1002 / lipi.19530550704 .
- ↑ В. Лангенбек, В. Прицков: Исследования механизма окисления парафинов, 2-я часть. В: жиры, мыло, краски . 55, 1953, стр. 506, DOI: 10.1002 / lipi.19530550805 .
- ^ A b c Михали Фройнд, Дьюла Мозес: Парафиновые продукты: свойства, технологии, применение. Elsevier Science Ltd., 1983, ISBN 978-0-444-99712-8 , стр. 64.
- ↑ Вильгельм Прицков: Об самоокислении кетонов, I. Ч.: Окисление циклогексанона. В: Химические отчеты . 87, 1954, стр. 1668, DOI: 10.1002 / cber.19540871110 .
- ↑ Т.О. Башкиров, В. Камзолкин: Синтез высших алифатических спиртов прямым окислением парафиновых углеводородов. В: Proc. World Pet. Cong. , 4, 1959, с. 175-183 ( аннотация ).
- ↑ Ф. Новак, В. Камзолкин, Ю. Талызенков, А. Башкиров: Механизм действия борной кислоты на жидкофазное окисление парафиновых углеводородов. В: Нефтехимия СССР 7, 1967, с. 59-64, DOI: 10.1016 / 0031-6458 (67) 90010-X .
- ^ Вильгельм Кейм, Арно Бер и Гюнтер Шмитт: Основы промышленной химии. Технические продукты и процессы, Отто Салле Верлаг, 1985, ISBN 3-7935-5490-2 , стр. 124-125.
- ^ W. Zenker: Инфракрасный метод прямого контроля окисления парафина и воска в присутствии борной кислоты. В: жиры, мыло, краски . 77, 1975, стр. 221-224, DOI: 10.1002 / lipi.19750770605 .
- ↑ К. Вайссермель, Х.-Дж. Арпе: Промышленная органическая химия: важные предварительные и промежуточные продукты. Wiley-VCH, 2007, ISBN 978-3-527-31540-6 , стр. 243-244.